题目内容
通过分析表格,总结规律及含义是培养学生能力的重要手段.下表是“部分酸、碱、盐在
20℃时的溶解性”.
(1)
查: 的溶解性为________.
的溶解性为________.
(2)
写化学式:一种酸________;一种不溶于水的盐________.(3)
判断:氯化钠溶液与硝酸钙溶液能否发生反应________(填“能”或“不能”);其理由是________.(4)
写化学方程式:铁或铝与表中的一种盐反应________.(5)
由上表可总结:碱中只有________不溶.(6)
下列各组离子不能共存的是[
]|
A .    |
B .    |
|
C .    |
D .    |
答案:略
解析:
解析:
|
(1) 不溶于水(2) 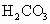 或 或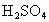 ), ),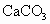 (或 (或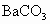 或 或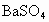 ……) ……)
(3) 不能,不符合复分解反应发生的条件(或生成物无水、无沉淀也无气体)(4) (5) (6)B (1) 在表格的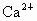 和 和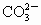 所在的横行和纵行、交叉处即为 所在的横行和纵行、交叉处即为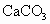 的溶解性,可知其不溶于水.(2)酸由 的溶解性,可知其不溶于水.(2)酸由 和酸根离子组成,表格中酸有HCl、 和酸根离子组成,表格中酸有HCl、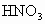 、 、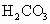 、 、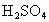 .不溶于水的物质表格中共有五种为 .不溶于水的物质表格中共有五种为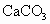 、 、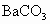 、 、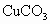 、 、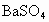 、 、 ,其中 ,其中 为碱,其余为盐,可任写上述四种盐中的一种.(3)判断NaCl与 为碱,其余为盐,可任写上述四种盐中的一种.(3)判断NaCl与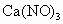 能否反应,要查阅表格判断 能否反应,要查阅表格判断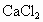 和 和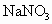 是否可溶于水,NaCl与 是否可溶于水,NaCl与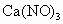 混合后无沉淀生成,不反应.(4)金属与盐的反应要注意金属必须排在盐中金属的前面,所以此表中只有铜盐可以选用,盐还必须可溶于水,因此满足条件的盐有 混合后无沉淀生成,不反应.(4)金属与盐的反应要注意金属必须排在盐中金属的前面,所以此表中只有铜盐可以选用,盐还必须可溶于水,因此满足条件的盐有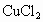 、 、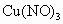 、 、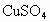 ,可选择其中的一种写其与Fe或Al的反应方程式.(5)碱是由金属离子和 ,可选择其中的一种写其与Fe或Al的反应方程式.(5)碱是由金属离子和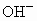 组成的,查表中 组成的,查表中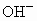 竖行可知 竖行可知 为难溶的碱.(6)离子相互组合后如果有沉淀、气体或水生成,离子就不能够共存.B项中 为难溶的碱.(6)离子相互组合后如果有沉淀、气体或水生成,离子就不能够共存.B项中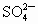 与 与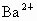 会结合成 会结合成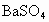 白色沉淀,所以 白色沉淀,所以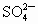 与 与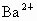 不能共存. 不能共存. |

练习册系列答案
相关题目
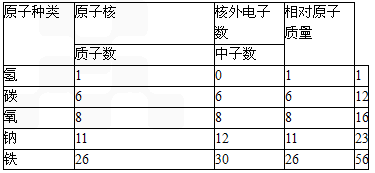
下表列出了初中化学里所学过的几种重要元素的原子结构:
分析表格栏目的内容及数据,你可以总结的规律
(1)______
(2)______
(3)______
(4)______
(5)______.
| 原子种类 | 原子核 | 核外电子 数 | 相对原子 质量 | |
| 质子数 | 中子数 | |||
| 氢 | 1 | 1 | 1 | |
| 碳 | 6 | 6 | 6 | 12 |
| 氧 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 12 | 11 | 23 |
| 铁 | 26 | 30 | 26 | 56 |
(1)______
(2)______
(3)______
(4)______
(5)______.
 (
(
 的溶解性为________.
的溶解性为________.