题目内容
【题目】实验室给你提供了下列仪器,请选用合适的仪器完成指定的实验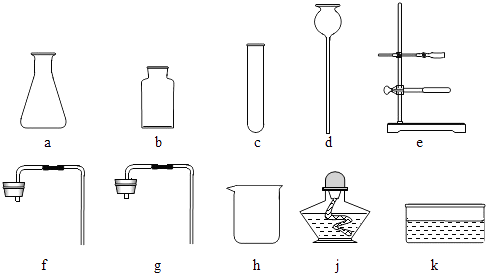
(1)①要制取较多的O2用来探究其性质(要求制取过程中可以添加反应物),组装气体发生装置需要的仪器是(填序号),收集氧气应采用法.
②提纯初盐时,过滤需要选用上述仪器中的(填序号),出此之外还缺少的仪器是滤纸、、(填名称).
(2)美羊羊同学的购物袋装薯片中发现还有一个小袋,上面标有“成分:CaO、Fe;作用:防潮、防氧化;警告:禁止食用”等字样,撕开小袋,发现里面的固体粉末有少许是棕红色,大多数是灰白色的.经过分析,她认为棕红色粉末是Fe2O3 , 灰白色粉末应该含有CaCO3和Fe,为验证自己的判断,美羊羊同学打算进行实验探究,请你一同参与.
【实验目的】证实灰白色粉末中含有CaCO3和Fe.
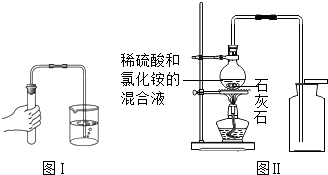
【实验设计】装置如图所示:
【实验预测与分析】
①若要证实样品中含有CaCO3 , 观察到的实验现象是 ,B中发生反应的化学方程式为 .
②若要证实样品中含有Fe,E中应该观察到的现象是 ,此时C装置的作用是
③看了美羊羊同学的分析结论,有同学认为小袋内灰白色粉末中还应该有别的物质,请你写出其中一种物质的化学式 .
【答案】
(1)a、d、f;向上排空气或排水;e、h;漏斗;玻璃棒
(2)样品表面有气泡产生,并且B中的澄清石灰水变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O;无水硫酸铜由白色变成蓝色;干燥气体;Ca(OH)2
【解析】解:(1)①制取较多的O2 , 应用锥形瓶,制取过程中可以添加反应物,应用长颈漏斗.并用f封闭锥形瓶和导出气体.因氧气的密度大于空气的密度,并不易溶于水,所以可以用向上排空气法或排水法收集气体.
所以答案是:a、d、f;向上排空气或排水;②过滤要用到的仪器有:铁架台、烧杯、漏斗、玻璃棒等.(2)①若样品中含有CaCO3 , CaCO3能与盐酸反应生成二氧化碳气体,观察到的实验现象是样品表面有气泡产生;生成的气体二氧化碳进入B,与其中的其中的澄清石灰水反应,化学反应式是:CO2+Ca(OH)2=CaCO3↓+H2O.
所以答案是:样品表面有气泡产生;CO2+Ca(OH)2=CaCO3↓+H2O.②若样品中含有Fe,Fe与盐酸反应生成氢气,氢气到达D装置后还原氧化铜,同时有水蒸气生成,水蒸气进入E装置,我们可以看到E中的无水硫酸铜变蓝;C装置中浓硫酸具有很好的吸水性,可用来干燥气体.
所以答案是:无水硫酸铜由白色变成蓝色;干燥气体;③因为小袋上面标有成分:CaO、Fe,其中的CaO会吸收空气中的水分,生成Ca(OH)2 , 所以灰白色粉末中还应该有Ca(OH)2 .
所以答案是:Ca(OH)2 .
【考点精析】解答此题的关键在于理解氧气的制取装置的相关知识,掌握发生装置:固固加热型、固液不加热型,以及对氧气的收集方法的理解,了解收集装置:根据物质的密度、溶解性;排水法收集时,待气泡均匀连续冒出时再收集(刚开始排出的是试管中的空气;)用排空气法收集气体时,导管伸到集气瓶底部.

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案