题目内容
【题目】请你根据下图回答下列问题:

A B C D E F
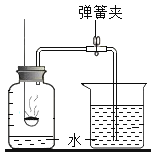
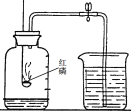
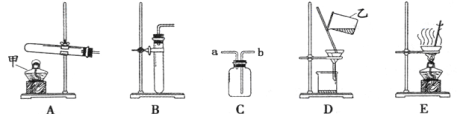
(1)某同学称取了15g高锰酸钾粉末,欲用装置F收集并测量产生氧气的体积,请选择发生装置 (填仪器编号)与F装置的接口代号正确连接:发生装置接口( )接( ),( )接 (填仪器名称)。发生装置中反应的符号表达式为: ;
(2)常温下,用锌粒和稀硫酸(液态)反应制取氢气,可选用的制取装置是 (填仪器编号),该装置虽操作简便,但无法控制产生氢气的速率。可选择图中 (填序号)装置来取代装置中的单孔塞,以达到控制产生氢气速率的目的。
【答案】(1)A adc 量筒 KMnO4 ![]() K2MnO4+MnO2+O2
K2MnO4+MnO2+O2
(2)BD或BE Ⅱ
【解析】
试题分析:(1)气体发生装置的选择依据:反应物的状态和反应条件,用高锰酸钾加热制取氧气属于“固固加热型”,故选择发生装置A;用装置F收集并测量产生氧气的体积,即要将水排出,气体应从短管(d端)进气,故发生装置与F装置的接口代号正确连接:a、d、c,最后连接量筒,通过读取量筒内水的体积即氧气体积,发生装置中反应的符号表达式为:KMnO4![]() K2MnO4+MnO2+O2
K2MnO4+MnO2+O2
(2)用锌粒和稀硫酸(液态)反应制取氢气,属于“固液常温型”,故可选用的发生装置是B;气体收集装置的选择依据:气体的密度和溶解性,由于氢气的密度比空气小,且难溶于水,故可采用向下排空气法和排水法,故制取装置是BD或BE;要达到控制产生氢气速率的目的,应选装置Ⅱ,可以通过控制滴加液体的速率来控制反应速率

【题目】归纳与反思是学习化学的重要环节。下列归纳完全正确的是
A.性质与用途 | B.营养与健康 |
氧气有助燃性—作燃料 熟石灰呈碱性—改良酸性土壤 石墨有导电性—用于制作电极 | 人体缺乏维生素A—易患夜盲症 水产品防腐—用甲醛水溶液浸泡 人体缺碘—易患甲状腺肿大 |
C.物质的鉴别 | D.物质与微粒构成 |
软水与硬水—肥皂水 天然纤维和合成纤维—灼烧 黄金和假黄金—观察颜色 | 金刚石—由碳原子构成 氧气—由氧分子构成 氯化钠—由Na+和Cl-构成 |