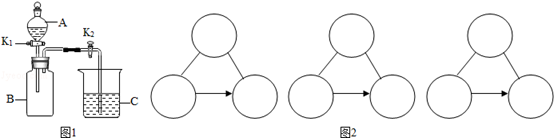
题目内容
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.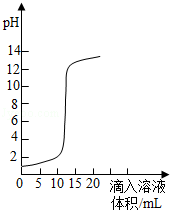
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH 7(填“大于”或“小于”或“等于”)
(2)根据曲线图判断,该反应是将 (填“氢氧化钠溶液”或“盐酸”,下同)滴入 中,理由是 .
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为 l (写化学式),若在此溶液中滴入石蕊试液,溶液显 色.
(1)等于;(2)氢氧化钠溶液;盐酸;在未滴入溶液之前,溶液的pH为1,酸性溶液;
(3)NaCl、HCl;红.
解析试题分析:(1)氢氧化钠和盐酸恰好完全反应时,氢离子和氢氧根离子均无剩余,溶液显中性,pH=7,故答案为:等于;(2)根据图象,在反应未进行时,溶液的pH=1,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入盐酸中,故答案为:氢氧化钠溶液;盐酸;在未滴入溶液之前,溶液的pH为1,酸性溶液;(3)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为5mL时,溶液仍为强酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸,酸使石蕊显红色,故答案为:NaCl、HCl;红.
考点:中和反应及其应用;溶液的酸碱性与pH值的关系.

 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案维生素C(简称Vc,又名抗坏血酸),易溶于水,易被氧化。人体缺乏Vc可能引发多种疾病。水果和蔬菜中含有丰富的Vc。某研究性学习小组对它探究如下:
探究一:测定饮料中Vc的含量。
【查阅资料】Vc能和高锰酸钾反应,使紫色的高锰酸钾溶液褪色。
【设计方案】分别向盛有1 mL等浓度高锰酸钾稀溶液的四支试管中逐滴滴加果味饮料、苹果汁、梨汁和0.04%的Vc溶液,边滴边振荡,直至高锰酸钾溶液褪色。
【实验数据】
| | 果味饮料 | 苹果汁 | 梨汁 | 0.04%的Vc溶液 |
| 滴加的滴数 | 40 | 10 | 20 | 5 |
【实验结论】分析数据可知,Vc含量最高的是 ,含量为 (各液体密度上的差别和每一滴的体积差别忽略不计)。
探究二:蔬菜放置时间的长短对其Vc含量是否有影响。
【设计方案】请你用新鲜的黄瓜、放置一周的黄瓜、高锰酸钾稀溶液和必要的仪器设计实验方案: 。
【实验结论】按上述方案实验,根据 这一实验结果,分析得出蔬菜放置时间的长短对其Vc的含量有影响。
【实验反思】化学实验需要控制变量。下列情况不会影响到测定结果的是 。
A.每次实验所用的果汁颜色不同
B.量取的被测物质的体积不同
C.试管的大小不同
D.没有用同一规格胶头滴管滴加
下表是几种家用清洁剂的功能、有效成分。
| 清洁剂名称 | 洁厕灵 | 活氧彩漂 | 漂白精 |
| 功 能 | 有效清除污垢,除异味 | 漂洗衣物,使色彩更鲜艳 | 快速漂除衣物污渍 |
| 有效成分 | HCl | H2O2 | NaClO |
据表回答下列问题:
(1)“洁厕灵”能否与碱性清洁剂混用? 。
(2)“洁厕灵”勿用于大理石清洁的理由是 。在盛有少量“活氧彩漂”液体的试管中,加少量二氧化锰,观察到的现象是 。
(3) “洁厕灵”与“漂白精”不能混用。二者若混合易产生一种有毒气体,化学方程式为:NaClO + 2HCl =" NaCl" + X↑ + H2O,则X的化学式为 。
某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示.
| 试剂 | 稀盐酸 | 食醋 | 蔗糖水 | 蒸馏水 | 肥皂水 | 烧碱溶液 | 石灰水 |
| 颜色 | 红 | 红 | 黄 | 黄 | 绿 | 绿 | 绿 |
请分析上表,并回答下列问题:
(1)该花汁 (填“可以”或“不可以”)作酸碱指示剂.
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的 .
(3)胃酸的主要成分是盐酸,胃舒平(主要成分Al(OH)3)和小苏打常用于治疗胃酸过多症,写出小苏打治疗胃酸过多症时的化学反应方程式 .
(4)石灰水暴露于空气中易变质,写出变质反应的化学方程式: .