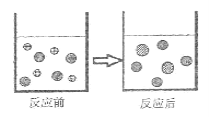
题目内容
【题目】氧化亚铜(Cu2O)可用于生产船底防污漆,防止海生物对船舶设备的污损。现将Cu2O和Cu的固体混合物20g放入烧杯中,加入质量分数为24.5%的稀硫酸50g,恰好完全反应。已知:Cu2O+H2SO4═CuSO4+Cu+H2O.计算:
(1)所加稀硫酸中溶质的质量为_____g。
(2)原混合物中Cu2O与Cu的质量比_____(写出计算过程,结果用最简整数比表示)
(3)在图中画出向20g Cu2O和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,铜的质量变化曲线_____。
【答案】12.25 9:1 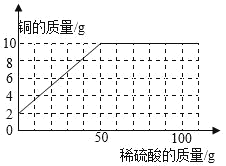 。
。
【解析】
根据加入的硫酸中溶质的质量和对应的化学方程式求算氧化亚铜的质量,进而求算对应的比值以及画图。
(1)所加稀硫酸中溶质的质量为24.5%×50g=12.25g;故填:12.25
(2)设原混合物中Cu2O的质量为x,生成的铜的质量为y。
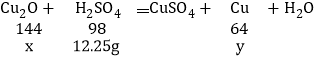
![]() 解得:x=18 g;y=8g;
解得:x=18 g;y=8g;
原混合物中Cu2O与Cu的质量比为18 g:(20 g﹣18 g)=9:1;故填:9:1
(3)没加入硫酸时,铜的质量为2g,加入到50g稀硫酸时铜的质量为2g+8g=10g。如下图所示;
 故填:
故填:

【题目】用珍珠加工成的“珍珠粉”是一种名贵中药材、保健品,可近年来市场上出现了一些假冒的“珍珠粉”,仅用肉眼观察难辨真假.为了向消费者提供鉴别方法,须找出真假“珍珠粉”理化性质上的差异.为此,某工商局提供了真、假“珍珠粉”样品和有关真假珍珠粉的资料如表:
品种 | 外观 | 成分 | 制作过程 |
真珍珠粉 | 白色无味粉末 | 主要为碳酸钙,可能含少量碳酸镁、壳角蛋白等. | 直接将珍珠磨成粉末. |
假珍珠粉 | 白色无味粉末 | 贝壳粉(主要成分为CaCO3),可能含少量碳酸镁并掺有少量淀粉. | 将贝壳漂白(漂白过程中用到过NaOH),然后磨成粉末. |
其中,真珍珠粉中的壳角蛋白(蛋白质的一种)不溶于水,加入浓硝酸加热后会变黄色.某研究性学习小组对提供的真假珍珠粉进行了如下探究.
(探究一)对真假珍珠粉的初步鉴定:
(1)真、假珍珠粉均属于_____(“纯净物”或“混合物”).取少量珍珠粉样品于试管中,加入_____并加热,若观察到变黄色,则该样品是真珍珠粉.
(2)另取少量市售廉价珍珠粉于试管中,加入足量水振荡后静置,将上层清液分别倒入2支试管中,向一支试管中滴加_____,混合液变成蓝色,说明其中掺有淀粉;再向另一支试管中加入1~2滴_____,溶液变成微红色,说明在漂白贝壳的过程中用到过氢氧化钠,使溶液呈碱性.
(探究二)测定市售珍珠粉中碳酸钙的质量分数:
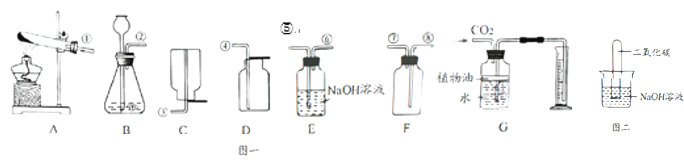
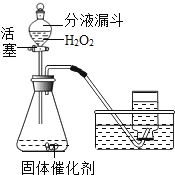
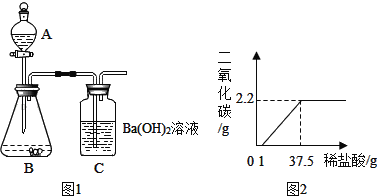
步骤Ⅰ:连接仪器组成如图1所示实验装置.某学生堵住C末端玻璃导管口,在A中装入少量水并取下上部塞子,打开玻璃活塞,A中水不能全部滴下,你认为该装置是否漏气?_____(填“漏气”或“不漏气”)
步骤Ⅱ:准确称取5.00g珍珠粉样品装入仪器B中,在A中装入一定浓度的稀盐酸.
步骤Ⅲ:向B中珍珠粉样品中滴加足量的稀盐酸.在仪器B、C中可观察到的现象分别为_____、_____.
步骤Ⅳ:完全反应后C中的混合液经_____、_____、干燥,称得白色固体的质量为9.85g(不考虑装置中原有空气及装置外空气的影响),由此求得珍珠粉样品中碳酸钙的质量分数为100%.
(实验反思)这个测定结果令研究小组的同学们感到难以理解,经过讨论分析,大家认为可能的原因是_____.(填数字序号)
①样品中含有碳酸镁 ②盐酸未滴加足量
③CO2气流速度太快导致未被Ba(OH)2完全吸收 ④装置B中水蒸气、HCl等进入装置C中
(拓展延伸)同学们根据测定数据计算出样品中碳酸根离子的质量分数为_____%.
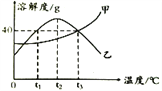
有同学提出在探究二中不需要装置C,只要用电子天平准确称量装置A、B反应前后的总质量,也可以求得珍珠粉样品中碳酸根离子的质量分数.你认为这样求得的碳酸根离子的质量分数与上面所得数值相比,将会_____(填“不变”、“偏大”或“偏小”).后来,同学们经过精确测定,得到所加稀盐酸与产生的二氧化碳气体质量关系如图2所示.
(分析讨论)
(1)在加入稀盐酸的过程中,开始没有气体产生,是因为固体样品中还含有少量_____(填“碳酸镁”或“氢氧化钠”)的缘故.
(2)根据图示,求出所用稀盐酸的溶质质量分数____?(需有计算过程)