题目内容
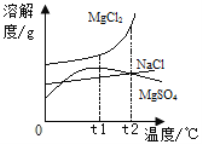
【题目】现有一包固体粉末,可能含有![]() 中的一种或几种。进行如下实验:
中的一种或几种。进行如下实验:
(1)取少量固体溶于足量水中,过滤得到白色固体A和无色滤液B,则原固体中一定不含有________.
(2)向固体A中加入足量稀盐酸,固体全部溶解,无气泡产生,则原固体中一定含有____________一定不含有______________。
(3)向滤液B中通入![]() ,产生白色沉淀,则原固体中一定还含有_______,一定不含有______。
,产生白色沉淀,则原固体中一定还含有_______,一定不含有______。
【答案】CuSO4 BaCO3 NaOH和Mg(NO3)2 BaCl2 K2SO4
【解析】
(1)硫酸铜溶液是蓝色,取少量固体溶于水,过滤得白色沉淀A和无色滤液B,则原固体中一定不含CuSO4;
(2)硝酸镁与氢氧化钠反应生成氢氧化镁沉淀和硝酸钠,氢氧化镁与盐酸反应生成可溶性的氯化镁和水,碳酸钡与盐酸反应生成氯化钡、水和二氧化碳,硫酸钾与氯化钡反应生成硫酸钡沉淀和氯化钾,硫酸钡不溶于稀盐酸。取固体A,加入足量稀HCl,固体完全溶解,无气泡产生,则原固体一定不含BaCO3,一定含有NaOH和Mg(NO3)2,K2SO4和BaCl2两种至少有一种不存在;
(3)氢氧化钠与二氧化碳反应生成碳酸钠和水,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠。向滤液B中通入CO2 ,产生白色沉淀,则原固体中一定还含有BaCl2,一定不含有K2SO4。

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案【题目】某兴趣小组同学对实验室制取氧气的催化剂进行如下探究:
(提出问题)二氧化锰常作为氯酸钾分解制取氧气的催化剂,其他氧化物是否也能催化氯酸钾分解呢?
(查阅资料)研究表明,许多金属氧化物对氯酸钾的分解(分解时放出热量)有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 | |
开始反应(℃) | 420 | 515 | 305 | 490 |
剧烈反应(℃) | 490 | 540 | 350 | 545 |
(1)实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的金属氧化物是_____。
(设计并完成实验)Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰混合均匀加热
Ⅲ.将Xg氯酸钾与1.0g氧化铜混合均匀加热
(2)实验Ⅲ中X的值应为_____,实验_____和Ⅲ比较可证明氧化铜能加快氯酸钾的分解速率。
(实验现象分析)将实验Ⅲ反应后的固体加水溶液、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同。
(3)在相同温度下比较两组实验产生氧气的快慢,通常可采用的方法有_____。
(结论)氧化铜也能做氯酸钾分解的催化剂。
(4)实验Ⅲ反应的文字表达式为_____。
注意:若答对第(5)小题奖励4分,化学试卷总分不超过60分。
(5)氯酸钾分解制取氧气的快慢还与哪些因素有关?请你提出新的合理的假设和实验方案。
(假设)_____。
(实验方案)_____。
(结论)_____。