题目内容
200mL质量百分比浓度为60%的浓硫酸(ρ=1.5g/mL)溶液的质量是 克,其中的溶质H2SO4占 克.
考点:有关溶质质量分数的简单计算
专题:溶液的组成及溶质质量分数的计算
分析:根据公式:m=ρv来计算溶液质量,溶质质量=溶液质量×溶质的质量分数来解答;
解答:解:浓硫酸溶液的质量是:200ml×1.5g/ml=300g;
其中的溶质H2SO4的质量:300g×60%=180g;
答案:300;180.
其中的溶质H2SO4的质量:300g×60%=180g;
答案:300;180.
点评:本题考查物质的量浓度有关计算,比较基础,侧重对基础知识的巩固,注意对公式的理解与灵活运用.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
化学反应遵循质量守恒定律,其原因是反应前后的( )
| A、分子种类没有改变 |
| B、分子数目没有改变 |
| C、原子种类和数目没有改变 |
| D、物质种类没有改变 |
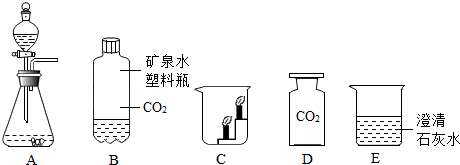
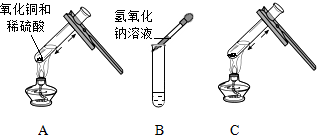
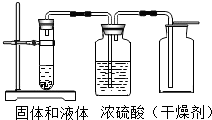 根据如图装置请你回答:
根据如图装置请你回答: