题目内容
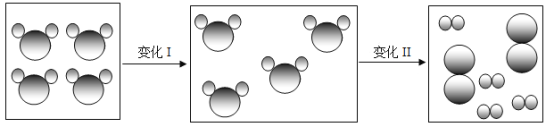
【题目】(1)小明在家做蔗糖溶于水的实验,现象如图所示。请从微观角度回答:
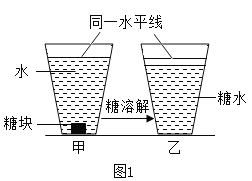
①乙中糖水属于混合物的理由是____。
②溶解后,乙中液面低于甲中液面的原因是____。
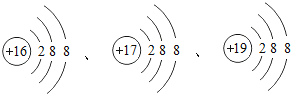
(2)硝酸钾和氯化铵的溶解度曲线如图1所示。
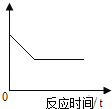
R是硝酸钾或氯化铵中的一种。某化学小组进行了如图2所示实验。
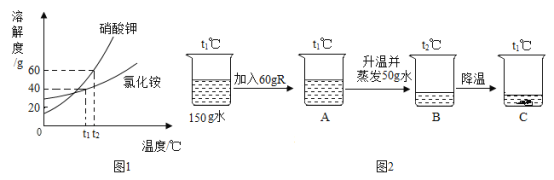
①溶解在水的溶质R是___(“硝酸钾”或“氯化铵”)。
②A、B、C中的溶液是饱和溶液的有______。
③B中溶液的溶质质量分数为___。
④使C中的固体溶解,可采用的方法是____。
【答案】糖水中含有两种分子(蔗糖分子和水分子) 分子之间有间隔 硝酸钾 B、C 37.5﹪ 加水(或升高温度)
【解析】
(1)用微观的知识分析,混合物是由不同种分子构成的。乙中糖水属于混合物是由于糖水中有糖分子和水分子。
(2)糖溶解前后对比,乙中液面低于甲中液面的原因是分子之间有间隔,糖分子和水分子相互进入对方分子的间隔中,导致溶液体积变小。
(3)从图示分析,在t1℃时,150g水是溶解了60gR,当温度升高到t2℃时,水蒸发了50g,溶液中没有固体析出,那么100g水完全溶解了60gR,可以推测R的溶解度![]() ,而在t2℃时氯化铵的溶解度小于60g,硝酸钾的溶解度等于60g,所以溶解在水的溶质R是硝酸钾。
,而在t2℃时氯化铵的溶解度小于60g,硝酸钾的溶解度等于60g,所以溶解在水的溶质R是硝酸钾。
(4)以上分析可知R为硝酸钾,在t1℃时,硝酸钾的溶解度大于40g,可推知150g水溶解硝酸钾的质量大于60g,则A为不饱和溶液;在t2℃时,硝酸钾的溶解度等于60g ,那么100 g水最多能溶解硝酸钾的质量为60g,则 B为饱和溶液;在t1℃时,C中的溶液中有硝酸钾固体未溶解完,则C是饱和溶液。所以A、B、C中的溶液是饱和溶液的有B、C。
(5)在t2℃时,B为饱和溶液,则溶液的溶质质量分数为![]()
(6)硝酸钾的溶解度随温度的升高而增大,使C中的固体溶解,可采用的方法是升高溶液的温度或向溶液中加入适量的水。

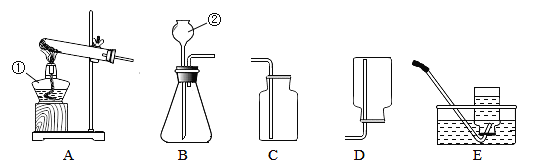
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
实 验 装 置 |
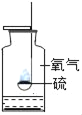
硫在氧气中燃烧 |
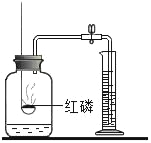
测定空气中氧气含量 |
测定空气中氧气含量 |
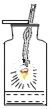
铁丝在氧气中燃烧 |
解释 | 集气瓶中的水: 吸收放出的热量 | 集气瓶中的水: 更快地吸收白烟 | 量筒中的水: 通过水体积的变化得出氧气体积 | 集气瓶中的水: 冷却溅落融熔物,防止集气瓶炸裂 |
A | B | C | D |
A. AB. BC. CD. D
【题目】水泥厂化验室为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量的 10% 的稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水)。有关实验数据如下表: 请计算:
反应前 | 反应后 | ||
实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
268.8g | 20g | 282.2g | |
(1)理论上得到二氧化碳气体_____克;
(2)该石灰石样品中中碳酸钙的质量分数_____。