题目内容
实验室有3瓶没有标签的无色溶液,小伟等3位同学组成化学实验小组来鉴别这些溶液.
(1)据实验室的老师说,这3瓶溶液可能是CuSO4、Na2CO3、KOH、HNO3溶液中的3种,同学们思考后,当即否定了CuSO4溶液,原因是______.
(2)同学们把3种溶液分别贴上A、B、C标签,按以下步骤进行探究:
第1步:分别用pH试纸测定3种溶液的酸碱度,方法为:______.
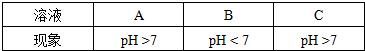
实验现象如下:
实验结论:B溶液是______.
第2步:取2支试管,分别加入少量的A、C溶液,然后依次滴加Ca(OH)2溶液,实验现象如下:
实验解释:C溶液中发生反应的方程式为:______.
实验结论:A溶液是______.
(3)老师提示:鉴别出B溶液后,不需外加试剂,就可简便地鉴别出A、C溶液,请完成下列实验报告:
(4)小伟说:“A和B溶液完全反应后所得的溶液中的溶质还是农作物生长所需的肥料呢!”请问,该肥料属于______(选填“氮肥”“磷肥”“钾肥”“复合肥”)
(1)据实验室的老师说,这3瓶溶液可能是CuSO4、Na2CO3、KOH、HNO3溶液中的3种,同学们思考后,当即否定了CuSO4溶液,原因是______.
(2)同学们把3种溶液分别贴上A、B、C标签,按以下步骤进行探究:
第1步:分别用pH试纸测定3种溶液的酸碱度,方法为:______.
实验现象如下:
| 溶液 | A | B | C |
| 现象 | pH>7 | pH<7 | pH>7 |
第2步:取2支试管,分别加入少量的A、C溶液,然后依次滴加Ca(OH)2溶液,实验现象如下:
| 溶液 | A | C |
| 现象 | 无明显现象 | 产生白色沉淀 |
实验结论:A溶液是______.
(3)老师提示:鉴别出B溶液后,不需外加试剂,就可简便地鉴别出A、C溶液,请完成下列实验报告:
| 实验步骤 | 实验现象和结论 |
| ______ | ______ |
(1)因为硫酸铜溶液呈蓝色,这与无色溶液不相符,故可排除硫酸铜溶液的可能;
(2)第1步:测定溶液pH的方法:用玻璃棒沾取溶液涂在试纸上,与标准比色卡对比,读数;Na2CO3、KOH、HNO3三种无色溶液中只有HNO3呈酸性,因此,根据pH测定结果可判断B溶液为稀硝酸;
第2步:根据碳酸钠溶液能与氢氧化钙溶液形成白色沉淀而氢氧化钾溶液不能与氢氧化钙发生反应,可判断加入氢氧化钙溶液产生白色沉淀的为碳酸钠溶液,反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;另一溶液即A溶液为氢氧化钾溶液;
(3)利用碳酸钠能与硝酸反应放出气体二氧化碳而氢氧化钾与硝酸反应无明显现象,可向两溶液中滴加B溶液稀硝酸鉴别剩余的两溶液;
(4)A溶液氢氧化钾溶液与B溶液硝酸溶液反应生成硝酸钾,硝酸钾既可提供作物生长所需的钾元素又能提供作物生长所需的氮元素,硝酸钾可作为复合肥;
故答案为:
(1)硫酸铜溶液呈蓝色;
(2)第1步:用玻璃棒沾取溶液涂在试纸上,与标准比色卡对比,读数;HNO3溶液;第2步:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;KOH溶液;
(3)
(4)复合肥.
(2)第1步:测定溶液pH的方法:用玻璃棒沾取溶液涂在试纸上,与标准比色卡对比,读数;Na2CO3、KOH、HNO3三种无色溶液中只有HNO3呈酸性,因此,根据pH测定结果可判断B溶液为稀硝酸;
第2步:根据碳酸钠溶液能与氢氧化钙溶液形成白色沉淀而氢氧化钾溶液不能与氢氧化钙发生反应,可判断加入氢氧化钙溶液产生白色沉淀的为碳酸钠溶液,反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;另一溶液即A溶液为氢氧化钾溶液;
(3)利用碳酸钠能与硝酸反应放出气体二氧化碳而氢氧化钾与硝酸反应无明显现象,可向两溶液中滴加B溶液稀硝酸鉴别剩余的两溶液;
(4)A溶液氢氧化钾溶液与B溶液硝酸溶液反应生成硝酸钾,硝酸钾既可提供作物生长所需的钾元素又能提供作物生长所需的氮元素,硝酸钾可作为复合肥;
故答案为:
(1)硫酸铜溶液呈蓝色;
(2)第1步:用玻璃棒沾取溶液涂在试纸上,与标准比色卡对比,读数;HNO3溶液;第2步:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;KOH溶液;
(3)
| 实验步骤 | 实验现象和结论 |
| 分别取A、C两溶液于试管中,然后取B溶液稀硝酸分别滴入试管 | 有气泡产生,溶液为Na2CO3溶液 无明显现象,溶液为KOH溶液 |

练习册系列答案
相关题目
实验室有3瓶没有标签的无色溶液,小伟等3位同学组成化学实验小组来鉴别这些溶液.
(1)据实验室的老师说,这3瓶溶液可能是CuSO4、Na2CO3、KOH、HNO3溶液中的3种,同学们思考后,当即否定了CuSO4溶液,原因是______.
(2)同学们把3种溶液分别贴上A、B、C标签,按以下步骤进行探究:
第1步:分别用pH试纸测定3种溶液的酸碱度,方法为:______.
实验现象如下:
| 溶液 | A | B | C |
| 现象 | pH>7 | pH<7 | pH>7 |
第2步:取2支试管,分别加入少量的A、C溶液,然后依次滴加Ca(OH)2溶液,实验现象如下:
| 溶液 | A | C |
| 现象 | 无明显现象 | 产生白色沉淀 |
实验结论:A溶液是______.
(3)老师提示:鉴别出B溶液后,不需外加试剂,就可简便地鉴别出A、C溶液,请完成下列实验报告:
| 实验步骤 | 实验现象和结论 |
| ______ | ______ |
实验室有3瓶没有标签的无色溶液,小伟等3位同学组成化学实验小组来鉴别这些溶液.
(1)据实验室的老师说,这3瓶溶液可能是CuSO4、Na2CO3、KOH、HNO3溶液中的3种,同学们思考后,当即否定了CuSO4溶液,原因是______.
(2)同学们把3种溶液分别贴上A、B、C标签,按以下步骤进行探究:
第1步:分别用pH试纸测定3种溶液的酸碱度,方法为:______.
实验现象如下:
实验结论:B溶液是______.
第2步:取2支试管,分别加入少量的A、C溶液,然后依次滴加Ca(OH)2溶液,实验现象如下:
实验解释:C溶液中发生反应的方程式为:______.
实验结论:A溶液是______.
(3)老师提示:鉴别出B溶液后,不需外加试剂,就可简便地鉴别出A、C溶液,请完成下列实验报告:
(4)小伟说:“A和B溶液完全反应后所得的溶液中的溶质还是农作物生长所需的肥料呢!”请问,该肥料属于______(选填“氮肥”“磷肥”“钾肥”“复合肥”)
(1)据实验室的老师说,这3瓶溶液可能是CuSO4、Na2CO3、KOH、HNO3溶液中的3种,同学们思考后,当即否定了CuSO4溶液,原因是______.
(2)同学们把3种溶液分别贴上A、B、C标签,按以下步骤进行探究:
第1步:分别用pH试纸测定3种溶液的酸碱度,方法为:______.
实验现象如下:
| 溶液 | A | B | C |
| 现象 | pH>7 | pH<7 | pH>7 |
第2步:取2支试管,分别加入少量的A、C溶液,然后依次滴加Ca(OH)2溶液,实验现象如下:
| 溶液 | A | C |
| 现象 | 无明显现象 | 产生白色沉淀 |
实验结论:A溶液是______.
(3)老师提示:鉴别出B溶液后,不需外加试剂,就可简便地鉴别出A、C溶液,请完成下列实验报告:
| 实验步骤 | 实验现象和结论 |
| ______ | ______ |
实验室有3瓶没有标签的无色溶液,小伟等3位同学组成化学实验小组来鉴别这些溶液.
(1)据实验室的老师说,这3瓶溶液可能是CuSO4、Na2CO3、KOH、HNO3溶液中的3种,同学们思考后,当即否定了CuSO4溶液,原因是______.
(2)同学们把3种溶液分别贴上A、B、C标签,按以下步骤进行探究:
第1步:分别用pH试纸测定3种溶液的酸碱度,方法为:______.
实验现象如下:
实验结论:B溶液是______.
第2步:取2支试管,分别加入少量的A、C溶液,然后依次滴加Ca(OH)2溶液,实验现象如下:
实验解释:C溶液中发生反应的方程式为:______.
实验结论:A溶液是______.
(3)老师提示:鉴别出B溶液后,不需外加试剂,就可简便地鉴别出A、C溶液,请完成下列实验报告:
(4)小伟说:“A和B溶液完全反应后所得的溶液中的溶质还是农作物生长所需的肥料呢!”请问,该肥料属于______(选填“氮肥”“磷肥”“钾肥”“复合肥”)
(1)据实验室的老师说,这3瓶溶液可能是CuSO4、Na2CO3、KOH、HNO3溶液中的3种,同学们思考后,当即否定了CuSO4溶液,原因是______.
(2)同学们把3种溶液分别贴上A、B、C标签,按以下步骤进行探究:
第1步:分别用pH试纸测定3种溶液的酸碱度,方法为:______.
实验现象如下:
| 溶液 | A | B | C |
| 现象 | pH>7 | pH<7 | pH>7 |
第2步:取2支试管,分别加入少量的A、C溶液,然后依次滴加Ca(OH)2溶液,实验现象如下:
| 溶液 | A | C |
| 现象 | 无明显现象 | 产生白色沉淀 |
实验结论:A溶液是______.
(3)老师提示:鉴别出B溶液后,不需外加试剂,就可简便地鉴别出A、C溶液,请完成下列实验报告:
| 实验步骤 | 实验现象和结论 |
| ______ | ______ |