题目内容
【题目】李明收集到一瓶浑浊的长江水,他要模拟自来水厂的净水过程,最终制成自来水。其实验过程如图所示。请回答以下问题。
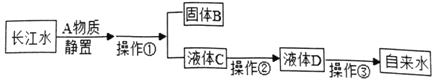
(1)操作①的名称是_____。用到的玻璃仪器有_____。
(2)操作②主要是除去水中的异味和色素,应选用的物质是_____。
(3)李明想知道净化后的D是不是硬水,检验的方法是:_____(写出步骤、现象及对应结论。)日常生活中常用_____的方法使硬水软化;
(4)操作③是消毒杀菌,这过程是_____变化(填“物理”或“化学”)。
(5)常用的杀菌消毒剂是高铁酸钠(化学式是Na2FeO4)试计算:
①高铁酸钠中各元素的质量比_____;
②多少克高铁酸钠中含有112克铁元素_____?
【答案】过滤 漏斗、烧杯、玻璃棒 活性炭 取适量的D倒入烧杯中,加入肥皂水,振荡,如泡沫丰富就是软水,如果浮渣较多就是硬水 煮沸 化学 23:28:32 332
【解析】
(1)操作①是固体和液体分离,为过滤,用到的玻璃仪器有漏斗、烧杯、玻璃棒;
(2)操作②主要是除去水中的异味和色素,应选用具有吸附性的活性炭;
(3)由于鉴别硬水和软水使用的是肥皂水,具体操作检验的方法是:取适量的D倒入烧杯中,加入肥皂水,振荡,如泡沫丰富就是软水,如果浮渣较多就是硬水。由于加热能将硬水转化为软水,所以日常生活中常用煮沸的方法使硬水软化;
(4)操作③是消毒杀菌,会生成新物质,所以这过程是化学变化。
(5)①高铁酸钠(化学式是Na2FeO4)钠元素、铁元素和氧元素的质量比为(23×2):56:(16×4)=23:28:32;
②高铁酸钠中铁元素的质量分数为![]() ,
,
需要高铁酸钠的质量为![]() 。
。

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目