��Ŀ����
����Ŀ����5�֣����ӹ�ҵ����30����FeCl3��Һ��ʴ������һ����ͭ�ľ�Ե�壬�Ƴ�ӡˢ��·��������Ϊ�˴ӷϸ�ʴҺ������CuCl2 ��FeCl2 ��FeCl3���л���ͭ���������õ�FeCl3��Һ���������ʵ�����̡�
��֪��2FeCl3 + Fe = 3FeCl2
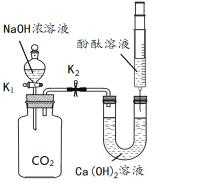
��1��������������������_______��
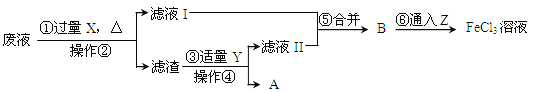
��2�����������У�X�Ļ�ѧʽΪ __ ��������������������_______�����������йط�Ӧ�Ļ�ѧ����ʽΪ_______��
��3��ZΪ�������ڢ������ķ�ӦΪ���Ϸ�Ӧ������Ӧ����ѧ����ʽΪ ��
���𰸡���1������
��2��Fe Fe ��Cu Fe + 2HCl === FeCl2 + H2��
��3��2FeCl2 + Cl2 === 2FeCl3
��������
�����������1���������������ǽ�Һ�������룬������������
��2���������ǽ�CuCl2 ��FeCl3ת��ΪFeCl2 �������������У�X�Ļ�ѧʽΪFe���������ӵ���ʱ�����ģ��������������������ǣ��������ɵ�ͭ�����й����������������������ǽ������й���������ȥ�������ӵ�����Y��Ϊ���ᣬ�ʷ����йط�Ӧ�Ļ�ѧ����ʽ Fe + 2HCl === FeCl2+H2��
��3��ZΪ���������ڢ������ķ�ӦΪ���Ϸ�Ӧ���ʽ�������غ㶨�ɣ���ѧ��Ӧǰ��Ԫ�ص�����䣬���ƶ�������ӦΪFeCl3������Ӧ����ѧ����ʽΪ2FeCl2+ Cl2=== 2FeCl3

 ��У����ϵ�д�
��У����ϵ�д�