题目内容
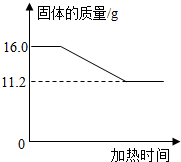 称取-定质量的氯酸钾和二氧化锰混合物,放人大试管中加热至质量不再变化为止. 实验测得固体混合物质量随加热时间变化的相关数据如图所示.请计算:
称取-定质量的氯酸钾和二氧化锰混合物,放人大试管中加热至质量不再变化为止. 实验测得固体混合物质量随加热时间变化的相关数据如图所示.请计算:(1)原混合物中氯酸钾的质量?
(2)下表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据
| 二氧化锰与氯酸钾的质量比 | 1/40 | 1/20 | 1/10 | 1/5 | 1/3 | 1/2 | 2/3 | 1/1 | 2/1 |
| 生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
②二氧化锰的用量过多时产生氧气的速率很慢,原因是
分析:(1)从图象中可以看出固体的质量在反应前后减少了,结合反应可知减少的质量即为气体的质量,可以据此求算
(2)①图表中可以分析出产生相同体积的气体所需时间最短的即为反应最快的
②二氧化锰的质量分数大冲淡了氯酸钾的粉末,速率变慢
(2)①图表中可以分析出产生相同体积的气体所需时间最短的即为反应最快的
②二氧化锰的质量分数大冲淡了氯酸钾的粉末,速率变慢
解答:解:(1)根据题意可知,固体质量减少的即为氧气的质量,可以根据氧气的质量结合化学方程式来解答
(2)①从图表中的数据分析可生成1L气体在质量比为1:10时反应速率最快
②若二氧化锰的比例太高可能会导致氯酸钾的质量相对过少而影响反应.
故答案为:(1)由题意可知生成氧气的质量为:16g-11.2g=4.8g,
设原混合物中氯酸钾的质量为X
2KClO3
2KCl+3O2↑
245 96
X 4.8g
=
解得:x=12.25g
(2)①1:10
②冲淡了氯酸钾粉末,相当于减少了反应物的质量分数
(2)①从图表中的数据分析可生成1L气体在质量比为1:10时反应速率最快
②若二氧化锰的比例太高可能会导致氯酸钾的质量相对过少而影响反应.
故答案为:(1)由题意可知生成氧气的质量为:16g-11.2g=4.8g,
设原混合物中氯酸钾的质量为X
2KClO3
| ||
| △ |
245 96
X 4.8g
| 245 |
| x |
| 96 |
| 4.8g |
解得:x=12.25g
(2)①1:10
②冲淡了氯酸钾粉末,相当于减少了反应物的质量分数
点评:主要考查了根据化学方程式进行相关的计算及质量守恒定律的应用,培养学生的应用知识的能力和解决问题的能力,要注意根据题给的数据进行分析得出已知量作为解题的依据.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
 完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数. 称取-定质量的氯酸钾和二氧化锰混合物,放入大试管中加热至质量不再变化为止. 实验测得固体混合物质量随加热时间变化的相关数据如图所示.请计算:原混合物中氯酸钾的质量?
称取-定质量的氯酸钾和二氧化锰混合物,放入大试管中加热至质量不再变化为止. 实验测得固体混合物质量随加热时间变化的相关数据如图所示.请计算:原混合物中氯酸钾的质量?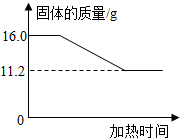 (2006?嘉兴)完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
(2006?嘉兴)完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.