题目内容
R的氧化物R2O3的式量为160,则相同价态的R的硝酸盐的式量为 ,相同物质的量的R的相同价态的氧化物和硝酸盐中的R元素的质量比为 .
考点:相对分子质量的概念及其计算,元素质量比的计算
专题:化学式的计算
分析:根据R氧化物的化学式计算出R元素的化合价以及相对原子质量,然后进行分析计算.
解答:解:设R的化合价为x,则2x+(-2)×3=0,x=+3,则其硝酸盐的化学式为:R(NO3)3;
根据“R的氧化物R2O3的式量为160”,则2R+16×3=160,解得R的相对原子质量为56.
则R的硝酸盐的式量为56+(14+16×3)×3=242.
相同物质的量的R的相同价态的氧化物和硝酸盐中的R元素的质量比1:1
故答案为:242;1:1.
根据“R的氧化物R2O3的式量为160”,则2R+16×3=160,解得R的相对原子质量为56.
则R的硝酸盐的式量为56+(14+16×3)×3=242.
相同物质的量的R的相同价态的氧化物和硝酸盐中的R元素的质量比1:1
故答案为:242;1:1.
点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、化学式的书写方法即可正确解答.

练习册系列答案
相关题目
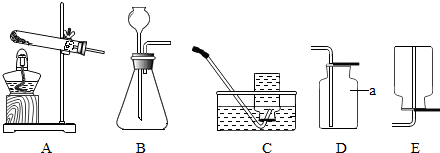
下列实验操作正确的是( )
A、 |
B、 |
C、 |
D、 |
 A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.