题目内容
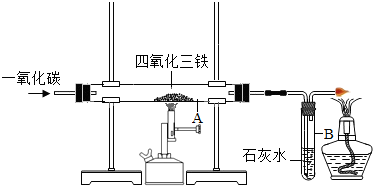
磁铁矿(主要成分Fe3O4)是炼铁的常用原料之一.下列是制取二氧化碳并进行有关物质性质实验的装置图,实验开始前要向装置中通入N2一会儿,防止空气中的氧气对实验有影响.请根据要求回答有关问题.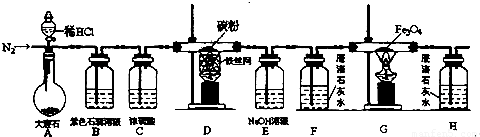
(1)装置A中发生的反应方程式为______.
(2)实验过程中装置B中的现象是______,装置H中的现象是______.
(3)实验结束后,在G装置玻璃管上方放一块磁铁,观察到的现象是______.
(4)写出下列装置中的化学方程式:装置G:______ 3Fe+4CO2
【答案】分析:(1)根据制取二氧化碳的原理分析;
(2)根据实验的设计结合化学方程式的书写分析;
(3)根据反应的生成物和磁铁的性质分析;
(4)根据实验的设计结合化学方程式的书写分析;
(5)根据一氧化碳排出污染空气进行分析.
解答:解:(1)装置A中是用大理石和稀盐酸制取二氧化碳,发生的反应方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红,因此实验过程中装置B中的现象是液体由紫色变红色;二氧化碳能使澄清的石灰水变浑浊,因此装置H中的现象是液体变浑浊.
(3)实验结束后,在G装置玻璃管上方放一块磁铁,磁铁会把生成的铁吸附到试管内壁的上部,因此观察到的现象是黑色粉末贴在玻璃管内壁的上部.
(4)装置G中发生的反应是一氧化碳还原四氧化三铁,该反应的化学方程式是4CO+Fe3O4 3Fe+4CO2;装置H中发生的反应是二氧化碳和氢氧化钙反应,该反应的化学方程式是:Ca(OH)2+CO2═CaCO3↓+H2O.
3Fe+4CO2;装置H中发生的反应是二氧化碳和氢氧化钙反应,该反应的化学方程式是:Ca(OH)2+CO2═CaCO3↓+H2O.
(5)该装置没有尾气处理装置,一氧化碳排出污染空气.
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)液体由紫色变红色;液体变浑浊;(3)黑色粉末贴在玻璃管内壁的上部;(4)4CO+Fe3O4 3Fe+4CO2;Ca(OH)2+CO2═CaCO3↓+H2O;(5)没有尾气处理装置,一氧化碳排出污染空气.
3Fe+4CO2;Ca(OH)2+CO2═CaCO3↓+H2O;(5)没有尾气处理装置,一氧化碳排出污染空气.
点评:本题考查了基本实验的设计,难度不大.注意在实验时一定要注意环保问题.
(2)根据实验的设计结合化学方程式的书写分析;
(3)根据反应的生成物和磁铁的性质分析;
(4)根据实验的设计结合化学方程式的书写分析;
(5)根据一氧化碳排出污染空气进行分析.
解答:解:(1)装置A中是用大理石和稀盐酸制取二氧化碳,发生的反应方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红,因此实验过程中装置B中的现象是液体由紫色变红色;二氧化碳能使澄清的石灰水变浑浊,因此装置H中的现象是液体变浑浊.
(3)实验结束后,在G装置玻璃管上方放一块磁铁,磁铁会把生成的铁吸附到试管内壁的上部,因此观察到的现象是黑色粉末贴在玻璃管内壁的上部.
(4)装置G中发生的反应是一氧化碳还原四氧化三铁,该反应的化学方程式是4CO+Fe3O4
 3Fe+4CO2;装置H中发生的反应是二氧化碳和氢氧化钙反应,该反应的化学方程式是:Ca(OH)2+CO2═CaCO3↓+H2O.
3Fe+4CO2;装置H中发生的反应是二氧化碳和氢氧化钙反应,该反应的化学方程式是:Ca(OH)2+CO2═CaCO3↓+H2O.(5)该装置没有尾气处理装置,一氧化碳排出污染空气.
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)液体由紫色变红色;液体变浑浊;(3)黑色粉末贴在玻璃管内壁的上部;(4)4CO+Fe3O4
 3Fe+4CO2;Ca(OH)2+CO2═CaCO3↓+H2O;(5)没有尾气处理装置,一氧化碳排出污染空气.
3Fe+4CO2;Ca(OH)2+CO2═CaCO3↓+H2O;(5)没有尾气处理装置,一氧化碳排出污染空气.点评:本题考查了基本实验的设计,难度不大.注意在实验时一定要注意环保问题.

练习册系列答案
相关题目