题目内容
【题目】乙醇俗称酒精,具有可燃性.甲、乙两组学生为了确定乙醇在氧气中燃烧的产物,他们分别先将乙醇在氧气中点燃,再用燃烧后的混合气体进行如下实验.实验中所用的新鲜鸭血是指先加入抗凝剂,再用水稀释后的鸭血,它遇O2呈深红色,遇CO2呈暗红色,遇CO呈鲜红色.甲、乙两组的实验顺序及观察到的现象如图所示(提示:白色无水硫酸铜吸水后变成蓝色)根据实验,回答下列问题: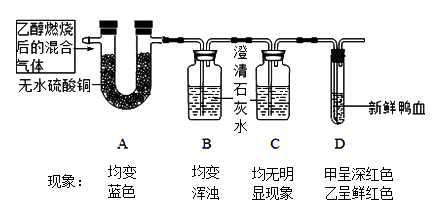
(1)甲小组确定乙醇燃烧的产物可是写出乙醇燃烧的化学反应方程式:;乙小组确定乙醇燃烧的产物可能是。
(2)分析甲、乙两个小组确定的产物为什么不同:。
(3)把A、B两个装置的顺序对调,行吗?为什么?。
(4)请你谈谈合理使用燃料的一种方法: 。
【答案】
(1)H2O 和CO2,C2H5OH + 3O2 ![]() 2CO2 + 3H2O,H2O 、CO2和CO
2CO2 + 3H2O,H2O 、CO2和CO
(2)甲组实验时氧气充足,乙醇能完全燃烧 乙组实验时氧气不充足,乙醇不完全燃烧
(3)不行,因为装置对调后无法证明乙醇燃烧的产物中是否有水
(4)使燃料充分燃烧(或提供足够多的空气,或氧气).
【解析】(1)甲小组的实验现象是无水硫酸铜变蓝,澄清石灰水变浑浊,说明乙醇燃烧生成了H2O和CO2 ,新鲜鸭血呈深红色,说明乙醇燃烧后的混合气体中含有氧气,即乙醇完全燃烧,乙醇完全燃烧的化学方程式是 C2H5OH + 3O2 ![]() 2CO2 + 3H2O 。乙小组的实验现象是无水硫酸铜变蓝,澄清石灰水变浑浊,新鲜鸭血呈鲜红色,说明乙醇燃烧生成了H2O、CO2 和CO;
2CO2 + 3H2O 。乙小组的实验现象是无水硫酸铜变蓝,澄清石灰水变浑浊,新鲜鸭血呈鲜红色,说明乙醇燃烧生成了H2O、CO2 和CO;
(2)含碳元素的物质充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳;
不能对调,因为澄清石灰水中含有水,装置对调后无法证明乙醇燃烧的产物中是否有水;
合理使用燃料即使燃料充分燃烧,增大燃料与空气的接触面积、提供足够多的空气都可以使燃料充分燃烧.
所以答案是:(1)H2O 和CO2;C2H5OH+3O2![]() 2CO2+3H2O; H2O、CO2 和CO;(2)甲组实验时氧气充足,乙醇能完全燃烧,乙组实验时氧气不充足,乙醇不完全燃烧;(3)不行,因为装置对调后无法证明乙醇燃烧的产物中是否有水;(4)使燃料充分燃烧(或提供足够多的空气,或氧气).
2CO2+3H2O; H2O、CO2 和CO;(2)甲组实验时氧气充足,乙醇能完全燃烧,乙组实验时氧气不充足,乙醇不完全燃烧;(3)不行,因为装置对调后无法证明乙醇燃烧的产物中是否有水;(4)使燃料充分燃烧(或提供足够多的空气,或氧气).
【考点精析】认真审题,首先需要了解书写化学方程式、文字表达式、电离方程式(注意:a、配平 b、条件 c、箭号),还要掌握甲烷、乙醇等常见有机物的性质和用途(甲烷的化学式: CH4(最简单的有机物,相对分子质量最小的有机物)物理性质:无色,无味的气体,密度比空气小,极难溶于水.化学性质:可燃性(发出蓝色火焰);乙醇 (俗称:酒精, 化学式:C2H5OH)化学性质:可燃性;工业酒精中常含有有毒的甲醇CH3OH,故不能用工业酒精配制酒)的相关知识才是答题的关键.

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案【题目】下列归类正确的是( )
选项 | 归类 | 物质 |
A | 黑色固体 | 高锰酸钾、四氧化三铁、炭黑 |
B | 可直接加热的仪器 | 试管、蒸发皿、玻璃棒 |
C | 刺激性气味的气体 | 氨气、二氧化硫、氦气 |
D | 缓慢氧化 | 铁丝生锈、农家肥的腐熟、天然气燃烧 |
A.AB.BC.CD.D
