题目内容
在学习化学过程中,我们会发现许多具有一定规律的知识.下面是某同学学习酸、碱、盐知识时总结的规律,其中错误的是( )
分析:根据已有的知识进行分析,电离时生成的阴离子全部是氢氧根离子的物质是碱;酸和碱能发生中和反应;酚酞试液在碱性溶液中变红,石蕊试液在碱性溶液中变蓝;盐酸能与某些活泼金属以及碳酸盐反应产生气体,据此解答.
解答:解:A、电离时生成的阴离子全部是氢氧根离子的物质是碱,氢氧根是由氢元素和氧元素组成的,故碱的组成中一定含有氢氧元素,故A正确;
B、酸能与碱发生中和反应,故能与碱发生中和反应的物质一定是酸,故B正确;
C、酚酞试液在碱性溶液中变红,能使无色酚酞溶液变红色的溶液呈碱性,石蕊试液在碱性溶液中变蓝,故能使无色酚酞溶液变红色的溶液一定能使紫色石蕊溶液变蓝色,故C正确;
D、碳酸盐能与盐酸反应产生二氧化碳气体,活泼金属能与盐酸反应生成氢气,向固体中加入稀盐酸,有气泡生成,该固体中不一定含有碳酸盐,故D错误;
故选D.
B、酸能与碱发生中和反应,故能与碱发生中和反应的物质一定是酸,故B正确;
C、酚酞试液在碱性溶液中变红,能使无色酚酞溶液变红色的溶液呈碱性,石蕊试液在碱性溶液中变蓝,故能使无色酚酞溶液变红色的溶液一定能使紫色石蕊溶液变蓝色,故C正确;
D、碳酸盐能与盐酸反应产生二氧化碳气体,活泼金属能与盐酸反应生成氢气,向固体中加入稀盐酸,有气泡生成,该固体中不一定含有碳酸盐,故D错误;
故选D.
点评:本题考查了对常见概念的理解,完成此题,可以依据已有的知识进行.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
在学习化学过程中,小强采用如下实验验证二氧化碳与氢氧化钠溶液确实发生了反应并作出了小结,请你帮他将实验报告部分内容补充完整(实验如下表所示):
| 方案 | 实验步骤 | 实验现象 |
| 1 | 取两个等体积的软塑料瓶,充满二氧化碳,然后________ ________. | ________ |
| 2 | 先将二氧化碳通入盛有足量氢氧化钠溶液的试管中,然后________ ________. | ________ |
小结:上述三个实验告诉我们:当某些化学反应现象不明显的化学反应,可以通过改变实验装置,创设新的情景来观察到明显反应的发生;对于无明显现象的化学反应,也可以从检验生成物的存在来判断反应的发生;对比实验是学习化学,开展探究的有效方法.
在学习化学过程中,小强采用如下实验验证二氧化碳与氢氧化钠溶液确实发生了反应并作出了小结,请你帮他将实验报告部分内容补充完整(实验如下表所示):
我能写出实验中方案2所涉及到的两个化学方程式 ,.我认为方案1的探究方法是 ,方案2的探究方法是 .
小结:上述三个实验告诉我们:当某些化学反应现象不明显的化学反应,可以通过改变实验装置,创设新的情景来观察到明显反应的发生;对于无明显现象的化学反应,也可以从检验生成物的存在来判断反应的发生;对比实验是学习化学,开展探究的有效方法.
| 方案 | 实验步骤 | 实验现象 |
| 1 | 取两个等体积的软塑料瓶,充满二氧化碳,然后 . | |
| 2 | 先将二氧化碳通入盛有足量氢氧化钠溶液的试管中,然后 . |
小结:上述三个实验告诉我们:当某些化学反应现象不明显的化学反应,可以通过改变实验装置,创设新的情景来观察到明显反应的发生;对于无明显现象的化学反应,也可以从检验生成物的存在来判断反应的发生;对比实验是学习化学,开展探究的有效方法.
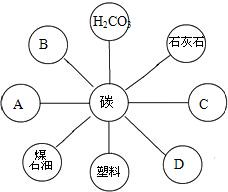 20、低碳生活(low-carbon life)不仅是当今社会的流行语,更是关系到人类未来的战略选择.碳和碳的化合物是化学世界中最庞大的家族,在学习化学的过程中我们结识了许多碳家族的成员.
20、低碳生活(low-carbon life)不仅是当今社会的流行语,更是关系到人类未来的战略选择.碳和碳的化合物是化学世界中最庞大的家族,在学习化学的过程中我们结识了许多碳家族的成员.