题目内容
 水是人类生活中不可缺少的物质.
水是人类生活中不可缺少的物质.(1)水是化学实验中常用的物质,请写出符合要求的化学式表达式
①有水参加的化合反应
CO2+H2O=H2CO3
CO2+H2O=H2CO3
②有水生成的分解反应
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
| ||
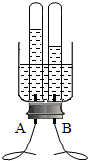
(2)小花同学设计了电解水简易装置.通电后的现象如图所示,则A是
正
正
极.电解水的化学式表达为2H2O
2H2↑+O2↑
| ||
2H2O
2H2↑+O2↑
.实验时还需在水中放入少量稀硫酸,作用是
| ||
增强水的导电性
增强水的导电性
.(3)实验时B管中产生的气体与A管中产生的气体体积比往往大于2:1,可能的原因是
氧气在水中的溶解性比氢气强
氧气在水中的溶解性比氢气强
.(4)电解水时,将
电能
电能
转化为化学能.电解36克水能得到氢气4
4
克.(化学变化中,反应前后元素质量不变)分析:(1)根据化合反应和分解反应的特征写出相应的化学方程式;
(2)根据电解水的现象回答:正氧负氢,氢二氧一;为增强水的导电性,要加入少量的稀硫酸或氢氧化钠;
(3)氢气和氧气的溶解性和溶解度等方面进行分析;
(4)根据反应条件及能量的转化分析;根据化学反应前后元素的质量不变计算.
(2)根据电解水的现象回答:正氧负氢,氢二氧一;为增强水的导电性,要加入少量的稀硫酸或氢氧化钠;
(3)氢气和氧气的溶解性和溶解度等方面进行分析;
(4)根据反应条件及能量的转化分析;根据化学反应前后元素的质量不变计算.
解答:解:(1)①有水参加的化合反应:如:CO2+H2O=H2CO3;②有水生成的分解反应,如:2H2O2
2H2O+O2↑;
(2)A试管中产生的气体较少,是氧气,在正极产生;反应的化学方程式为:2H2O
2H2↑+O2↑;因为纯水不易导电,要加入少量的稀硫酸增强水的导电性;
(3)氢气难溶于水,氧气不易溶于水,可见氧气与氢气相比,氧气更易溶于水,所以实验时B管中产生的氢气与A管中产生的氧气体积比往往大于2:1;
(4)电解水是在直流电的作用下发生化学变化,故是将电能转化成化学能;根据化学反应前后元素的质量不变,故水中氢元素的质量为:36g×
×100%═4g;
故答案为:(1)①CO2+H2O=H2CO3(合理即可);②2H2O2
2H2O+O2↑(合理即可)
(2)正 极; 2H2O
2H2↑+O2↑; 增强水的导电性;
(3)氧气在水中的溶解性比氢气强 或在电极上反应了部分氧气(答一即可).
(4)电能; 4.
| ||
(2)A试管中产生的气体较少,是氧气,在正极产生;反应的化学方程式为:2H2O
| ||
(3)氢气难溶于水,氧气不易溶于水,可见氧气与氢气相比,氧气更易溶于水,所以实验时B管中产生的氢气与A管中产生的氧气体积比往往大于2:1;
(4)电解水是在直流电的作用下发生化学变化,故是将电能转化成化学能;根据化学反应前后元素的质量不变,故水中氢元素的质量为:36g×
| 2 |
| 18 |
故答案为:(1)①CO2+H2O=H2CO3(合理即可);②2H2O2
| ||
(2)正 极; 2H2O
| ||
(3)氧气在水中的溶解性比氢气强 或在电极上反应了部分氧气(答一即可).
(4)电能; 4.
点评:本题以水为载体考查了水的电解的现象、原理及误差分析等,属于基础性的考查,要求学生在平时的学习中要扎实基础.

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目