题目内容
镀金铁画中只含有金、铁、碳三种元素,某同学为探究镀金铁画中三种元素的含量,进行了如下实验:取镀金铁画的边角料6g,磨成粉末,放入足量的稀盐酸中,收集到0.2g氢气,溶液过滤后,将残渣洗净、烘干,在空气中充分灼烧,剩余固体的质量为0.24g.试计算:
(1)镀金铁画样品中含金的质量
(2)镀金铁画样品中铁的质量分数?(结果保留到0.1%)
(1)镀金铁画样品中含金的质量
(2)镀金铁画样品中铁的质量分数?(结果保留到0.1%)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:因为金、铁、碳这三种元素,只有铁可以和盐酸发生反应,产生氢气,故可根据化学方程式得出反应物之间的比例式,求出铁的质量;由题意可知,溶液过滤后,将残渣洗净、烘干,在空气中充分灼烧,剩余固体的质量为0.24g.因为金的硬度高,性质稳定,所以剩余固体就是金.
解答:解:(1)由题意可知,溶液过滤后,将残渣洗净、烘干,在空气中充分灼烧,剩余固体的质量为0.24g.因为金的硬度高,性质稳定,所以剩余固体就是金,因此,镀金铁画样品中含金的质量为0.24g;
故答案为:0.24g;
(2)因为金、铁、碳这三种元素,只有铁可以和盐酸发生反应,产生氢气,故可根据化学方程式得出反应物之间的比例式,求出铁的质量.
解:设6.0g铁画边角料中所含铁的质量为x
Fe+2HCl=FeCl2+H2↑
56 2
x 0.2g
=
解之得x=5.6g
铁的质量分数为:
×100%=93.3%.
答:镀金铁画样品中铁的质量分数为93.3%.
故答案为:0.24g;
(2)因为金、铁、碳这三种元素,只有铁可以和盐酸发生反应,产生氢气,故可根据化学方程式得出反应物之间的比例式,求出铁的质量.
解:设6.0g铁画边角料中所含铁的质量为x
Fe+2HCl=FeCl2+H2↑
56 2
x 0.2g
| 56 |
| 2 |
| x |
| 0.2g |
解之得x=5.6g
铁的质量分数为:
| 5.6g |
| 6g |
答:镀金铁画样品中铁的质量分数为93.3%.
点评:本题主要考查学生对物质质量分数的计算能力.学生必须熟知所给物质的性质,才能正确分析发生反应的过程,据此判计算物质质量,进而计算出质量分数.

练习册系列答案
相关题目
化学方程式可表明( )
①反应物和生成物各是什么,②符合质量守恒定律,③反应物和生成物之间的质量比,④反应物和生成物之间分子(或原子)数的关系.
①反应物和生成物各是什么,②符合质量守恒定律,③反应物和生成物之间的质量比,④反应物和生成物之间分子(或原子)数的关系.
| A、①② | B、①③ |
| C、③④ | D、①②③④ |
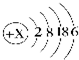 某元素原子结构示意图如图所示,
某元素原子结构示意图如图所示, 化学与生活息息相关,知识源于生活.
化学与生活息息相关,知识源于生活.