题目内容
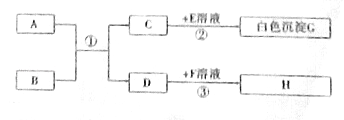
【题目】某化学兴趣小组为测定某有机物(含C、H、O三种元素)中各元素的质量比,用如图实验装置(部分夹持装置略去)进行探究. 
提示:装置C中发生的反应为2Na2O2+2CO2=2Na2CO3+O2
实验数据:
读数 | 反应前质量/g | 反应后质量/g |
电子天平a | 217.0 | 222.4 |
电子天平b | 150.0 | 158.4 |
请计算该有机物中各元素的质量比(写出计算过程).
【答案】解:反应生成水的质量为:222.4g﹣217.0g=5.4g,水中氢元素质量为:5.4g× ![]() ×100%=0.6g, C装置中增重:158.4g﹣150.0g=8.4g,
×100%=0.6g, C装置中增重:158.4g﹣150.0g=8.4g,
设有机物和氧气反应生成二氧化碳质量为x,
2Na2O2+ | 2CO2=2Na2CO3+ | O2 | C装置中增重质量 |
88 | 32 | 88﹣32=56 | |
x | 8.4g |
![]() =
= ![]() ,
,
x=13.2g,二氧化碳中碳元素质量为:13.2g× ![]() ×100%=3.6g,
×100%=3.6g,
则有机物中氧元素质量为:9.0g﹣3.6g﹣0.6g=4.8g,
该有机物中碳、氢、氧三种元素的质量比为:3.6g:0.6g:4.8g=6:1:8,
答:该有机物中碳、氢、氧三种元素的质量比为6:1:8
【解析】该有机物和氧气充分反应生成水和二氧化碳,装置B中的浓硫酸吸收反应生成的水,装置C中根据反应的化学方程式及其提供的数据可以计算二氧化碳的质量,进一步可以进行相关方面的计算和判断.
【考点精析】通过灵活运用根据化学反应方程式的计算,掌握各物质间质量比=系数×相对分子质量之比即可以解答此题.

练习册系列答案
相关题目