题目内容
【题目】小明同学欲通过化学实验证明“质量守恒定律”,确定以“稀盐酸与碳酸钠反应”为研究对象,设计的实验装罝如图所示.
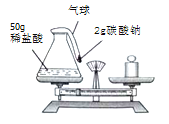
(1)根据实验目的,小明应该测量的数据是 (填“只有反应前”、“只有 反应后”、“反应前、后”之一)整个反应装罝(包括锥形瓶、气球和药品)的质量.
(2)实验步骤如下:
①按如图方式放好仪器,使天平平衡,记录称量数据.
②将碳酸钠粉末全部倒入锥形瓶中,观察到锥形瓶中液体里出现的现象是
③当反应结束时,气球已经完全鼓起,小明发现天平的指针巳经向右偏了。小明又重新称量,记录了数据。
他感到困惑:其他操作均正常,实验现象与数据为何与预测结果不符?你认为出现该实验现象的合理解释最应该是下列各项中的 (填序号)
A.该反应前后原子的种类、数目变少
B.该反应生成物的总质量小于反应物的总质量
C.空气的浮力作用干扰了实验结果
D.生成气体的反应不遵守质量守恒定律
【答案】(1)反应前、后 (2)有气泡产生 C
【解析】
试题分析:实验证明“质量守恒定律”必须通过测量反应前后的质量的变化来确定;将碳酸钠粉末全部倒入锥形瓶中,观察到锥形瓶中液体里出现的现象是有气泡产生;该实验虽然出现了天平的偏转,但是还是遵守质量守恒定律的,化学变化都是遵循质量守恒定律的,可能是气球中气体将球膨胀后,增大了浮力,使得结果出现偏差。

练习册系列答案
相关题目