题目内容
【题目】(某白色固体可能含有氯化钠、硫酸钠、碳酸钠中的一种或几种,现将该固体溶于水配成溶液后,甲同学进行了验证实验,过程如下:
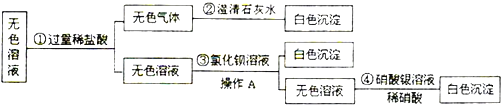
(1)由甲同学的实验过程可知,该白色固体中含有 _________ .(填名称,下同)写出无色气体与澄清石灰水反应的化学方程式 _________ .
(2)乙同学经过研究改换了上述实验中的①③两种试剂,除实验现象与甲同学的完全相同外,还将白色固体的成分确定了,则乙同学是把试剂①换成了 _________ ;把试剂③换成了 _________ ,该白色固体的组成 _________ .
【答案】(1)硫酸钠、碳酸钠 (2)CO2 +Ca(OH)2 ==CaCO3↓+ H20
(3)稀硝酸 硝酸钡溶液 (4)氯化钠、硫酸钠、碳酸钠
【解析】
试题分析:此题属于鉴别型框图推断题,解题时,要抓住特征现象,找到推断的题眼,采用顺藤摸瓜的方法可推得结论.本题主要考查了特征离子(碳酸根离子、硫酸根离子、氯离子)的检验
(1)在无色溶液中加入过量的稀盐酸,产生无色气体,通入澄清石灰水中,生成白色沉淀,说明一定含有碳酸钠,而实验③在无色溶液中,加入氯化钡溶液,产生白色沉淀,说明一定含有硫酸钠,故该白色固体中含有:硫酸钠、碳酸钠,无色气体与澄清石灰水反应的化学方程式:CO2 +Ca(OH)2 ==CaCO3↓+ H20
(2)第一种方案确定含有硫酸钠、碳酸钠,不能确定含有氯化钠,因为实验①加入过量的稀盐酸,在溶液中引入了氯离子,所以实验④,加入硝酸银溶液和稀硝酸,出现白色沉淀,并不能判断溶液中的氯离子是来自于原无色溶液中,还是加入的稀盐酸中,故为了判断氯化钠是否存在,在实验①和③中就不能引入氯离子,所以要得到实验现象与甲同学的完全相同外,还将白色固体的成分确定了,则乙同学是把试剂①换成了稀硝酸,把试剂③换成了硝酸钡溶液,这样最终就可以确定该白色固体的组成:氯化钠、硫酸钠、碳酸钠

【题目】(根据溶液的知识回答下列问题.
(1)20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到四个各盛有50g水的烧杯中,充分溶解,其溶解情况如表.根据表中数据回答下列问题:
物质 | 甲 | 乙 | 丙 | 丁 |
未溶解固体的质量/g | 4.2 | 2 | 0 | 9.2 |
①所得四杯溶液 _________ 不一定是饱和溶液(填序号,下同)
②所得四杯溶液中 _________ 的溶质质量分数最小.
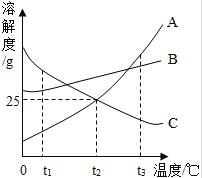
(2)如图是A、B、C三种物质的溶解度曲线,据图回答:
①t3℃时,将25gC放入100g水中,充分搅拌后得到C的饱和溶液,将其变为不饱和溶液的方法是 _________ ;
②t3℃时,将等质量A、B、C的饱和溶液降温至t2℃时,所得A、B、C的三种溶液中溶质质量分数由小到大的顺序是 _________ .