题目内容
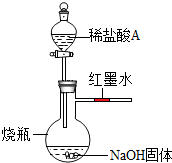 (2013?许昌二模)为了探究酸碱中和反应中是否放热,某同学设计了如图所示的实验装置.
(2013?许昌二模)为了探究酸碱中和反应中是否放热,某同学设计了如图所示的实验装置.(1)请你分析这个实验的不足之处?认为应该如何改进?
(2)改进试验后,观察到的什么现象说明中和反应放热?
分析:(1)氢氧化钠溶于水也会放出热量,所以不能用氢氧化钠固体来进行实验,应该选择氢氧化钠的浓溶液来进行实验,可以据此解答该题;
(2)反应若放出热量,则会使烧瓶中的气体受热而膨胀,从而将红墨水向右推移,可以据此解答.
(2)反应若放出热量,则会使烧瓶中的气体受热而膨胀,从而将红墨水向右推移,可以据此解答.
解答:解:(1)氢氧化钠溶于水也会放出热量,所以不能用氢氧化钠固体来进行实验,应该选择氢氧化钠的浓溶液来替换氢氧化钠固体来进行实验;
(2)反应若放出热量,则会使烧瓶中的气体受热而膨胀,从而将红墨水向右推移,所以若观察到红墨水右移,则说明中和反应放热.
故答案为:(1)用氢氧化钠的浓溶液来代替氢氧化钠固体进行实验;
(2)若观察到红墨水右移,则说明中和反应放热.
(2)反应若放出热量,则会使烧瓶中的气体受热而膨胀,从而将红墨水向右推移,所以若观察到红墨水右移,则说明中和反应放热.
故答案为:(1)用氢氧化钠的浓溶液来代替氢氧化钠固体进行实验;
(2)若观察到红墨水右移,则说明中和反应放热.
点评:要想解答好这类题目,首先,要理解和熟记中和反应及其应用等相关知识.然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目