题目内容
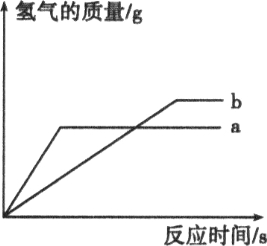
【题目】用质量相等的锌粉和铁粉,分别与溶质质量分数相同且等质量的稀盐酸充分发生反应,产生氢气的质量与时间的关系如图所示.
请回答下列问题:
(1)表示锌粉与稀盐酸反应的曲线为________(填“a”或“b”).
(2)对于a曲线表示的反应,________(填名称)有剩余.
【答案】(1)a (2)稀盐酸
【解析】(1)锌比铁活泼,与酸反应速率快,即在相同时间内产生氢气的质量大,所以曲线a为锌粉与稀盐酸反应的曲线.
(2)由图看出,锌最终产生的氢气质量比铁产生的少,铁、锌与盐酸反应的化学方程式分别为Fe+2HCl=FeCl2+H2↑、Zn+2HCl=ZnCl2+H2↑,由化学方程式中各物质间的质量可知,若酸完全反应,则生成的氢气质量相等;若相同质量的铁和锌完全反应,铁消耗的酸和产生的氢气质量比锌多.在题图所示情况下,与锌反应的稀盐酸有剩余.

练习册系列答案
相关题目