��Ŀ����
����Ŀ���̣�Mn����ά������������������������Ԫ�أ����̻�������������������Ҳ���㷺Ӧ�ã����ͼ����Ϣ������������ȷ���ǣ� �� 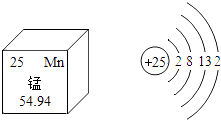
A.��ԭ�Ӻ�����25�����ӣ�һ����ԭ�ӵ�������54.94g
B.��ԭ�Ӻ�����4�����Ӳ㣬�仯ѧ���������ڲ���Ӿ���
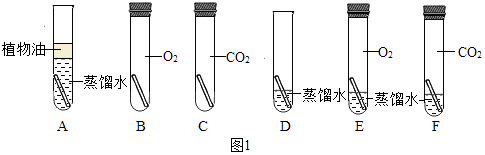
C.MnO2�����������H2O2�ֽ���O2��ʵ����������
D.KMnO4Ϊ�Ϻ�ɫ���壬������ˮ�����͵��ܼ����γ��Ϻ�ɫ��Һ
���𰸡�C
���������⣺A������Ԫ��Ԫ�����ڱ���һ�����Ϣ���Ͻǵ�����Ϊ25����ʾԭ������Ϊ25������ԭ������=�˵����=����������ԭ�Ӻ�����25�����ӣ�������������ֱ�ʾ���ԭ����������Ԫ�ص����ԭ������Ϊ54.94��������һ����ԭ�ӵ�������54.94g����ѡ��˵������ B������ԭ�ӵĽṹʾ��ͼ����ԭ�Ӻ�����4�����Ӳ㣻�仯ѧ������������������������ѡ��˵������
C����������������Ԫ���������һ������Ԫ�أ�������������������ڶ������̵Ĵ�����������ˮ��������������������������ѡ��˵����ȷ��
D��KMnO4Ϊ�Ϻ�ɫ���壬������ˮ�γ��Ϻ�ɫ��Һ�����������ͣ���ѡ��˵������
��ѡ��C��
A������ͼ��Ԫ�����ڱ����Ի�õ���Ϣ�����Ͻǵ����ֱ�ʾԭ��������������������ֱ�ʾ���ԭ�����������з����жϼ��ɣ�
B��ԭ�ӽṹʾ��ͼ�У�ԲȦ�����ֱ�ʾ���������������߱�ʾ���Ӳ㣬����Ԫ�ػ�ѧ���ʵ������������������з����жϣ�
C����������Ԫ����ɵĻ������У�����һ������Ԫ�ص����������Ϲ�������ֽ���ȡ�����ķ�Ӧԭ�������з����жϣ�
D�����ݸ�����ص��������ʽ��з����жϣ�