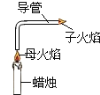
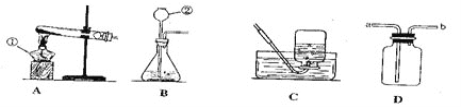
题目内容
【题目】如图是某省生产的某加钙食盐包装标签上的部分文字,请仔细阅读后回答问题:

![]() 包装标签上的钙含量是指________(单质/碳酸钙/钙元素)
包装标签上的钙含量是指________(单质/碳酸钙/钙元素)
![]() 为了测定此盐中的钙元素含量,取
为了测定此盐中的钙元素含量,取![]() 这种盐溶于水,加入足量的盐酸,生成
这种盐溶于水,加入足量的盐酸,生成![]() 二氧化碳,计算此加钙食盐中钙元素的质量分数.________
二氧化碳,计算此加钙食盐中钙元素的质量分数.________
【答案】钙元素 ![]()
【解析】
(1)食盐中的碳酸钙可起到补充人体所需钙元素,因此食盐成份表中标明的为钙元素的含量;
(2)碳酸钙含有碳酸根,能与酸反应放出二氧化碳,厨房中食醋中含有食醋,因此可选择食醋来检验食盐中的碳酸钙;
(3)设生成0.11g二氧化碳需要消耗碳酸钙质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 0.11g
![]() x=0.25g
x=0.25g
加钙食盐中钙元素的质量分数= ![]() = 1%。
= 1%。
答:此加钙食盐中钙元素的质量分数为1%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】小明对铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他把纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录。请你分析回答:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时的现象 | 剧烈燃烧, 无火星。 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | A_____ |
(1) 表中“A”处内容应为 ___________________。
(2)镁条燃烧的化学式表达式为__________________________。
(3)通过以上探究,你认为铁丝燃烧产生火星四射现象的原因可能是__________________;实验时,铁丝需绕成螺旋状的目的是______________________,为防止瓶底炸裂,需__________,铁丝燃烧的化学式表达式为____________________________________。
(4)铁除了可以在氧气中燃烧,还可以在空气中发生缓慢氧化,该过程 _________(填“放热”或“吸热”);在生活中缓慢氧化的例子很多,下列也属于缓慢氧化的是____(填序号)。
①锅炉爆炸 ②动植物的呼吸 ③食物的腐烂 ④水结成冰 ⑤酒和醋的酿造 ⑥农家肥的腐熟 ⑦火药爆炸
(5)某同学利用铁粉来测定空气中氧气的含量,如图所示,将足量的铁粉用水均匀地粘在试管内壁上,将试管倒立在装有水的烧杯中。实验过程中,观察到试管内液面缓慢上升。下列分析错误的是(______)
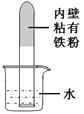
A.水能进入试管的最大体积为试管容积的1/5
B.该铁粉在试管内发生了氧化反应
C.这一实验可以验证空气的组成不是单一的
D.如果把铁粉改为木炭粉,两者的现象完全相同