题目内容
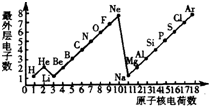 (2006?乌鲁木齐)如图是1~18号元素原子最外层电子数与原子核电荷数的关系图:
(2006?乌鲁木齐)如图是1~18号元素原子最外层电子数与原子核电荷数的关系图:试回答:
(1)6号元素属于
非金属
非金属
(填写“金属”或“非金属”);(2)17号元素的原子核外电子数为:
l7
l7
,它与氢元素所形成的化合物的化学式为HCl
HCl
;(3)请写出图中氦元素形成氦气的化学式
He
He
;(4)通过上图你能发现哪些规律?请你写出其中的一条:
随着原子核电荷数的递增,原子最外层电子数呈周期性变化
随着原子核电荷数的递增,原子最外层电子数呈周期性变化
.分析:(1)根据6号元素为碳元素进行判断;
(2)根据原子序数=核外电子数以及氯的化合价为-1价,氢的化合价为+1价进行解答;
(3)根据氦气是由原子直接构成的物质,然后确定物质的化学式;
(4)通过对该图的分析,总结归纳规律.
(2)根据原子序数=核外电子数以及氯的化合价为-1价,氢的化合价为+1价进行解答;
(3)根据氦气是由原子直接构成的物质,然后确定物质的化学式;
(4)通过对该图的分析,总结归纳规律.
解答:解:(1)6号元素为碳元素,属于非金属元素;
(2)原子序数=核外电子数,17号元素的原子核外电子数为:17;氯的化合价为-1价,氢的化合价为+1价,根据化合物中各元素的化合价的代数和为0可知,它与氢元素所形成的化合物的化学式为:HCl;
(3)氦气是由原子直接构成的物质,用元素符号表示该物质,所以氦气的化学式:He;
(4)通过对该图的分析,总结归纳规律:随着原子核电荷数的递增,原子最外层电子数呈周期性变化.
故答案为:(1)非金属;(2)17;HCl;(3)He;(4)随着原子核电荷数的递增,原子最外层电子数呈周期性变化.
(2)原子序数=核外电子数,17号元素的原子核外电子数为:17;氯的化合价为-1价,氢的化合价为+1价,根据化合物中各元素的化合价的代数和为0可知,它与氢元素所形成的化合物的化学式为:HCl;
(3)氦气是由原子直接构成的物质,用元素符号表示该物质,所以氦气的化学式:He;
(4)通过对该图的分析,总结归纳规律:随着原子核电荷数的递增,原子最外层电子数呈周期性变化.
故答案为:(1)非金属;(2)17;HCl;(3)He;(4)随着原子核电荷数的递增,原子最外层电子数呈周期性变化.
点评:本题考查学生利用图中的最外层电子数来分析元素,并利用最外层电子数来分析性质,能利用化合价来书写物质的化学式,注重了化学用语的训练.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目