题目内容
【题目】如下图是甲、乙两种固体物质的溶解度曲线。
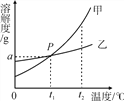
(1)由图可获得的一条信息是________。
(2)若乙中混有少量甲,提纯乙的方法是________。
(3)t2 ℃时,将不饱和的甲溶液,转化成该温度下的饱和溶液的一种方法是________。
(4)将等质量的甲、乙两种物质的溶液由t2 ℃降温至t1 ℃时,析出晶体的质量________(填序号)。
A.甲>乙 B.甲<乙 C.无法确定
【答案】 t1 ℃时,甲和乙的溶解度相等 蒸发结晶 加入溶质 C
【解析】根据已有的溶解度曲线的意义进行分析解答,交点表示在该温度下两种物质的溶解度相等;根据溶解度曲线可以看出物质的溶解度受温度的变化情况;结合饱和溶液和不饱和溶液的转化以及溶解度随温度的变化特点确定析出晶体的方法进行分析解答。(1)据图可以看出,在t1 ℃时,甲和乙的溶解度相等;(2)据图可以看出,乙的溶解度受温度影响变化不大,若乙中混有少量甲,可以使用蒸发结晶的方法提纯乙;(3)t 2℃时,将不饱和的甲溶液转化成该温度下的饱和溶液可以使用加入溶质的方法。变化过程中,溶质的质量分数将增大;(4)将等质量的甲、乙两种物质的溶液由t 2℃降温至t1 ℃时,由于不知道溶液是否饱和,故甲析出晶体的质量无法比较,故选C。

【题目】兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关探究。
[提出问题] 它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
[实验探究1] 向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下表:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠 溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 蓝紫色 | 蓝色 | 绿色 | 黄色 |
查阅资料:
pH | 7.5~9 | 10~11.9 | 12~14 |
紫甘蓝汁液 显示的颜色 | 蓝色 | 绿色 | 黄色 |
[得出结论1] 三种溶液的碱性由强到弱的顺序为______________________。
[实验探究2] 甲同学在烧杯中加入约5 mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由______色变为________色。向其中加入稀盐酸,该反应的化学方程式为___________。乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如下图甲所示。a点表示的含义是________________。
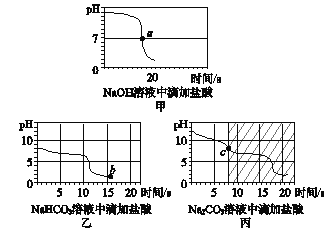
[得出结论2] 从微观角度分析,该反应的实质是_____________________。
[实验探究3] 向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图乙、图丙所示。
[交流与反思] b点的溶质为____________________。(填化学式),将图乙和图丙中的阴影部分进行叠加,发现两者基本重合,c点的溶质为____________(填化学式)。
[得出结论3] 通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表示:______、______________。
[结论与反思] 探究溶液的酸碱性及反应pH的变化,可以认识反应的原理及进行的过程。