题目内容
写出下列反应的化学方程式,并在括号里注明反应的基本类型:(1)氯酸钾与二氧化锰混合制氧气
(2)白磷在燃烧
(3)铝丝浸入硫酸铜溶液中
(4)二氧化硫通入氢氧化钠溶液中
分析:(1)①氯酸钾与二氧化锰混合制氧气:可知反应物氯酸钾、生成物氯化钾与氧气、反应条件,所以可以书写化学方程式;②分解反应:指一种化合物在特定条件下(如加热,通直流电,催化剂等)分解成二种或二种以上较简单的单质或化合物的反应;可简记为AB=A+B;
(2)①白磷在燃烧:可知反应物磷与氧气、生成物五氧化二磷、反应条件点燃,所以可以书写化学方程式;②化合反应:指的是由两种或两种以上的物质生成一种新物质的反应;可简记为A+B=AB;
(3)铝丝浸入硫酸铜溶液中,可知反应物铝与硫酸铜、生成物铜与硫酸铝,所以可以书写化学方程式;
(4)二氧化硫通入氢氧化钠溶液中,可知反应物二氧化硫与氢氧化钠、生成物亚硫酸钠与水,所以可以书写化学方程式.
(2)①白磷在燃烧:可知反应物磷与氧气、生成物五氧化二磷、反应条件点燃,所以可以书写化学方程式;②化合反应:指的是由两种或两种以上的物质生成一种新物质的反应;可简记为A+B=AB;
(3)铝丝浸入硫酸铜溶液中,可知反应物铝与硫酸铜、生成物铜与硫酸铝,所以可以书写化学方程式;
(4)二氧化硫通入氢氧化钠溶液中,可知反应物二氧化硫与氢氧化钠、生成物亚硫酸钠与水,所以可以书写化学方程式.
解答:解:(1)氯酸钾与二氧化锰混合制氧气:可知反应物为氯酸钾、生成物氯化钾和氧气、反应条件二氧化锰作催化剂、加热,故可以书写化学方程式2KClO3
2KCl+3O2↑;此反应符合AB=A+B,即“一变多”,故为分解反应;
(2)白磷在燃烧:可知反应物P与O2、生成物P2O5、反应条件点燃,故可以书写化学方程式4P+5O2
2P2O5;此反应符合A+B=AB,即“多变一”,故为化合反应;
(3)铝丝浸入硫酸铜溶液,可知反应物铝丝与硫酸铜、生成物铜与硫酸铝,故可以书写化学方程式2Al+3CuSO4=Al2(SO4 )3+3Cu;
(4)二氧化硫通入氢氧化钠溶液,知反应物二氧化硫与氢氧化钠、生成物Na2SO3、H2O,故化学方程式为2NaOH+SO2=Na2SO3+H2O
故答为:(1)2KClO3
2KCl+3O2↑;分解反应;(2)4P+5O2
2P2O5;化合反应;
(3)2Al+3CuSO4=Al2(SO4 )3+3Cu;(4)2NaOH+SO2=Na2SO3+H2O
| ||||
| 加热 |
(2)白磷在燃烧:可知反应物P与O2、生成物P2O5、反应条件点燃,故可以书写化学方程式4P+5O2
| ||
(3)铝丝浸入硫酸铜溶液,可知反应物铝丝与硫酸铜、生成物铜与硫酸铝,故可以书写化学方程式2Al+3CuSO4=Al2(SO4 )3+3Cu;
(4)二氧化硫通入氢氧化钠溶液,知反应物二氧化硫与氢氧化钠、生成物Na2SO3、H2O,故化学方程式为2NaOH+SO2=Na2SO3+H2O
故答为:(1)2KClO3
| ||||
| 加热 |
| ||
(3)2Al+3CuSO4=Al2(SO4 )3+3Cu;(4)2NaOH+SO2=Na2SO3+H2O
点评:本题主要考查了化学方程式的正确书写的方法步骤,掌握化和反应、和分解反应及其应用;学会反应类型的判定方法.

练习册系列答案
相关题目
(2009?娄底)小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
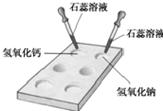
(1)如图所示,在白色点滴板上进行实验,请将实验现象填入下表:
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方 程式______.
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式______.
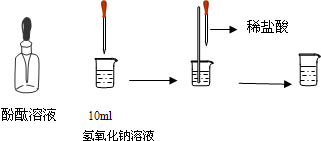
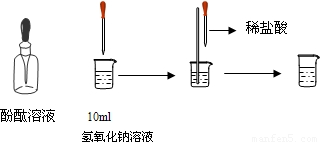
(4)如图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显______色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止.这一实验说明:酸与碱作用生成了盐和水,这一反应叫做______反应.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)?
①______
②______.
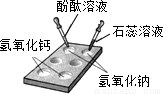
(1)如图所示,在白色点滴板上进行实验,请将实验现象填入下表:
| 氢氧化钠溶液 | 氢氧化钙溶液 | |
| 加紫色石蕊溶液 | ______ | ______ |
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式______.
(4)如图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显______色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止.这一实验说明:酸与碱作用生成了盐和水,这一反应叫做______反应.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)?
①______
②______.