题目内容
(2012?镇江)下列说法错误的是( )
分析:A、区分硬水和软水所含的钙镁离子多少不同,故常用肥皂水来区分;
B、根据硝酸铵与氢氧化钠溶于水温度变化区分;
C、根据食盐水和稀盐酸使指示剂变色情况区分;
D、根据聚氯乙烯与聚乙烯灼烧情况区分.
B、根据硝酸铵与氢氧化钠溶于水温度变化区分;
C、根据食盐水和稀盐酸使指示剂变色情况区分;
D、根据聚氯乙烯与聚乙烯灼烧情况区分.
解答:解:A、硬水含钙镁离子多,而软水含的钙镁离子少,所以当加入肥皂水后,硬水产生的泡沫少,而软水产生的泡沫多,故可鉴别;
B、硝酸铵溶于水时会吸收热量,使温度降低,氢氧化钠溶于水放出热量,使温度升高,故可鉴别;
C、食盐水呈中性,稀盐酸呈酸性,都不能使酚酞变色,故不能鉴别;
D、聚氯乙烯灼烧有臭味,而聚乙烯没有,故燃烧闻气味可以鉴别;
故选C.
B、硝酸铵溶于水时会吸收热量,使温度降低,氢氧化钠溶于水放出热量,使温度升高,故可鉴别;
C、食盐水呈中性,稀盐酸呈酸性,都不能使酚酞变色,故不能鉴别;
D、聚氯乙烯灼烧有臭味,而聚乙烯没有,故燃烧闻气味可以鉴别;
故选C.
点评:物质的鉴别是初中化学的难重点,也是中考的热点之一,熟练掌握物质的物理性质和化学性质,是解决问题的前提条件.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
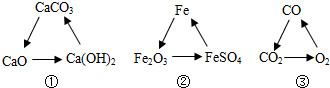
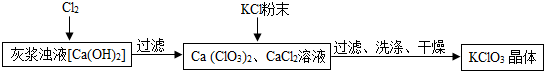
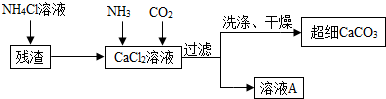


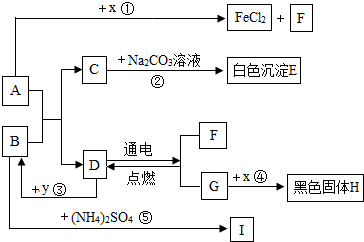 (1)B俗称
(1)B俗称