题目内容
结合下列实验装置,回答有关问题.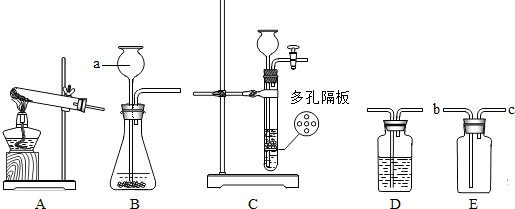
(1)若用高锰酸钾制取氧气,应选用的发生装置是
(2)若要制取二氧化碳,在B装置中装有石灰石,那么a中应加入
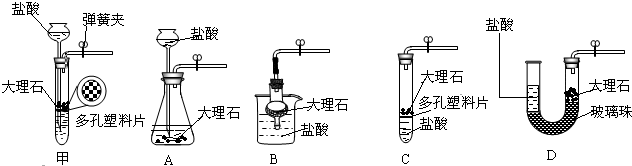
(3)实验室如用块状固体和液体无需加热制取难溶性气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是
(4)用D装置除去CO中混有的少量CO2气体,D中最好盛放
分析:实验室制取气体的发生装置选择的依据为反应物的状态和反应的条件,收集装置的选择依据气体本身的密度、溶解性等物理性质;用高锰酸钾制氧气的反应原理为2KMnO4
K2MnO4+MnO2+O2↑,实验室制取二氧化碳的反应原理为CaCO3+2HCl=CaCl2+CO2↑+H2O;装置E用于收集气体时收集密度大于空气密度的气体时应从长导管通入,收集密度小于空气密度的气体,应从短导管通入;装置C与启普发生器的原理相似,打开止水夹时液体药品与固体药品接触反应,关闭止水夹时生成的气体造成装置内压强增大,使两种药品分离停止反应;除去CO中混有的少量CO2气体应选择的物质能与二氧化碳反应,与一氧化碳不反应;能用于干燥二氧化碳气体的干燥剂应能与水蒸气反应或具有吸水性,且不与二氧化碳反应.
| ||
解答:解:(1)用高锰酸钾制氧气需要加热,因此应选择给固体加热的装置;用高锰酸钾制氧气的反应原理为2KMnO4
K2MnO4+MnO2+O2↑
(2)实验室制取二氧化碳的反应原理为CaCO3+2HCl=CaCl2+CO2↑+H2O;石灰石为固体稀盐酸为液体,因此应选择固液混合不加热型气体发生装置;二氧化碳密度大于空气密度;
(3)装置C打开止水夹时液体药品与固体药品接触反应,关闭止水夹时生成的气体造成装置内压强增大,使两种药品分离停止反应,能起到随时控制反应发生和停止的作用;
(4)氢氧化钠溶液能与二氧化碳反应,与一氧化碳不反应;浓硫酸具有吸水性且不与二氧化碳反应.
故答案为(1)A;2KMnO4
K2MnO4+MnO2+O2↑
(2)稀盐酸;CaCO3+2HCl=CaCl2+CO2↑+H2O;b
(3)控制反应发生和停止(或随开随用随关随停…)
(4)NaOH;浓H2SO4
| ||
(2)实验室制取二氧化碳的反应原理为CaCO3+2HCl=CaCl2+CO2↑+H2O;石灰石为固体稀盐酸为液体,因此应选择固液混合不加热型气体发生装置;二氧化碳密度大于空气密度;
(3)装置C打开止水夹时液体药品与固体药品接触反应,关闭止水夹时生成的气体造成装置内压强增大,使两种药品分离停止反应,能起到随时控制反应发生和停止的作用;
(4)氢氧化钠溶液能与二氧化碳反应,与一氧化碳不反应;浓硫酸具有吸水性且不与二氧化碳反应.
故答案为(1)A;2KMnO4
| ||
(2)稀盐酸;CaCO3+2HCl=CaCl2+CO2↑+H2O;b
(3)控制反应发生和停止(或随开随用随关随停…)
(4)NaOH;浓H2SO4
点评:气体的实验室制法主要从药品、反应原理、发生装置、收集装置、检验、验满及实验操作注意事项等方面进行比较、归纳,总结实验室制取气体的一般思路和方法.装置的改进和气体除杂质也是深入思考的重点.

练习册系列答案
相关题目
 “嫦娥一号”是我国自主研制、成功发射的第一个月球探测器.“嫦娥一号”的成功发射,使全国人民欢欣鼓舞.请同学们阅读下列短文并回答有关问题.
“嫦娥一号”是我国自主研制、成功发射的第一个月球探测器.“嫦娥一号”的成功发射,使全国人民欢欣鼓舞.请同学们阅读下列短文并回答有关问题.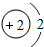 D.属于金属元素,在化学反应中易得到电子
D.属于金属元素,在化学反应中易得到电子
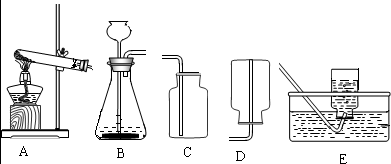
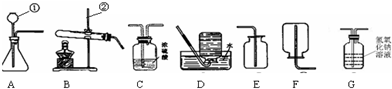
 (2)结合下列实验装置图回答问题:
(2)结合下列实验装置图回答问题: E.为了防止冷凝水回流,给试管中固体加热时,试管口略向下倾斜
E.为了防止冷凝水回流,给试管中固体加热时,试管口略向下倾斜