��Ŀ����
����Ŀ����ѧ������ʦ������һ��Сħ�����������С�����ͬ�����£���A��B���������ͬ�ļ���ƿ�зֱ������ɫ�����⣨H2S������Ͷ����������壮����ͼ��ʾ���鿪ë����Ƭ��ƿ�ڶԽ����ߵ����Σ�ʹ���������ֻ�ϣ�һ�������ƿ�ڱڿɼ����ŵ���ɫ�����������ش��������⣺
��1�����á��ʾ��ԭ�ӣ��á��ʾ��ԭ�ӣ���![]() ��ʾ��ԭ�ӣ�������Ӧ���̿�����ͼ��ʾ��ʾ��
��ʾ��ԭ�ӣ�������Ӧ���̿�����ͼ��ʾ��ʾ��
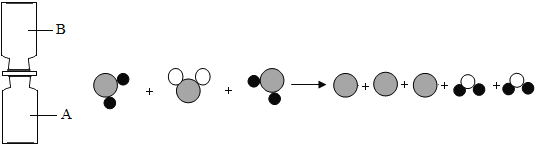
�÷�Ӧ�Ļ�ѧ����ʽΪ �����⡢������������Ԫ�صĻ��ϼ۷ֱ�Ϊ ��
��2�����������ƿ�����ʵؽ���������ƿ�����ǽ���۲쵽����ƿ����ˣ�ԭ���� ��
��3����֪����ͬ�����£������������������ķ�����Ŀ��ȣ���Ӧ��ϣ�ƿ��ʣ�������Ϊ ������������ķ����� ��
���𰸡���1��2H2S+SO2=3S+2H2O����2��+4��2��H2S��SO2��Ӧ�����ɹ�̬�����Һ̬��ˮ��ʹƿ�ڵ�ѹǿС��ƿ��Ĵ���ѹ����������ƿ����ˣ�3������������ƿ�ڵ���NaOH��Һ����
����������1�����ݷ�Ӧ����ͼʾ��ÿ2��H2S���ӿ���1��SO2���ӷ�Ӧ������������ԭ�Ӻ�����ˮ���ӣ��ݴ˿�д����ѧ����ʽ��2H2S+SO2=3S+2H2O��
��������Ԫ�صĻ��ϼ���+1�ۣ����������Ԫ�صĻ��ϼ�Ϊ��2�ۣ�������������Ԫ�صĻ��ϼ��ǩ�2�ۣ����������Ԫ�صĻ��ϼ�Ϊ+4�ۣ�
��2������ƿ����ˣ�ԭ���� H2S��SO2��Ӧ�����ɹ�̬�����Һ̬��ˮ��ʹƿ�ڵ�ѹǿС��ƿ��Ĵ���ѹ����������ƿ�����
��3����֪��ͬ�����£������������������ķ�����Ŀ��ȣ���ʣ�������Ķ����������壬���ն��������������������������Һ��

 ����������ϵ�д�
����������ϵ�д� �Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
�Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�����Ŀ���о���ѧϰС��ⶨʵ������һƿ���õ�NaOH�����Ƿ���ʣ�
��������⡿NaOH�����Ƿ���ʣ�
����������衿����1��û���ʣ�ȫ����NaOH��
����2��ȫ���ʣ�ȫ����Na2CO3
����3�����ֱ��ʣ��Ⱥ���NaOH���ֺ���Na2CO3��
����Ʒ���������ʵ�顿����������һ����ɣ����ش��������⣮
ʵ�鲽�� | ʵ������ | ʵ����� |
�ٳ�ȡ����������Ʒ8g����100mLˮ�����Һ������Һ�еμӹ������Ȼ�����Һ��ַ�Ӧ���ã� | ˵�����ù����У�һ������Na2CO3 | |
���ò�����պȡ�������е��ϲ���Һ����pH��ֽ�ϣ������ɫ���Աȣ����pH | pH=10 | ˵�������У���һ������ ���ѧʽ���� |
����������У��μӹ����Ȼ�����Һ��Ŀ����
��ʵ����ۡ�ͨ��ʵ�飬˵������������ ����ȷ�ģ�
����չ��
��1��Ϊ�ⶨ����NaOH����ı��ʳ̶ȣ�������������ɫ�������ˡ�ϴ��������Ƶ�������Ϊ2g���������Ʒ��NaOH����������Ϊ ���ٶ��Լ������������ʣ���
��2��Ҫ��ȥ���������к��е�̼���ƣ����õķ������û�ѧ����ʽ��ʾ��
����˼��ͨ��̽����ʵ�����е���������Ӧ�ܷⱣ�森