题目内容
(2011年福建龙岩,13题))在部分地区发生“抢盐”风波后,我国政府及时发布公告称:核事故对我国海域污染可能性极小,且我国85%以上的食盐是湖盐(来自内陆盐湖)而不是海盐。已知:盐湖原盐主要成分是NaCl,还含有泥沙和芒硝等。右图为芒硝和氯化钠的溶解度曲线。请回答: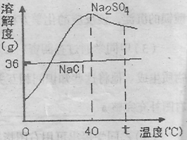
(1)将t℃饱和硫酸钠溶液降温至40℃时,溶液中 (填“有”、“没有”)晶体析出。
(2)为除去原盐中的泥沙,可先将原盐溶解,再通过 操作除去。
(3)可用“夏季采盐,冬季捞硝”的方法来分离湖水中的芒硝和食盐。这种方法的化学原理是 。
(1) 没有 (2)过滤 (3)氧化钠的溶解度受温度影响变化不大,硫酸钠的溶解度受温度影响变化较大
解析试题分析:(1)由于在40~t℃时,硫酸钠的溶解度随温度的降低而减小,因此将t℃饱和硫酸钠溶液降温至40℃时,饱和溶液就会变成不饱和溶液,溶液中不会有晶体析出,故答案为:没有,
(2)由于泥沙不易溶于水,而食盐能溶于水,因此可以通过过滤的方法除去泥沙,故答案为:过滤,
(3)由于食盐的溶解度受温度的影响很小,而硫酸钠的溶解度受温度的影响较大,因此由于夏季温度高,硫酸钠的溶解度大,随着水分的蒸发,氯化钠就会从溶液中结晶析出,而大多数硫酸钠仍旧会溶解在溶液中,而冬天时,温度低,硫酸钠的溶解度变得很小,就会从溶液中结晶析出,而氯化钠的溶解度受温度的影响很小,不会从溶液中结晶析出,因此夏天晒盐,冬天捞碱,故答案为:氯化钠的溶解度受温度影响变化不大,硫酸钠的溶解度受温度影响变化较大。
考点:此题考查的是固体溶解度曲线及其作用,过滤的原理、方法及其应用,结晶的原理、方法及其应用,晶体和结晶的概念与现象。
点评:本题难度不是很大,主要考查了固体溶解度曲线所表示的意义及根据固体的溶解度曲线解决相关的问题。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案