题目内容
一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示。下列关于以上反应的说法中,正确的是
| A.X的值为44 |
| B.W由碳、氢两种元素组成 |
| C.该反应属于置换反应 |
| D.W中碳、氢元素质量比为4:1 |
D
解析试题分析:根据质量守恒定律:参加化学反应的各物质质量总和等于反应后生成的各物质质量总和,利用在发生化学反应时反应物质量会减小,生成物质量会增多,判断反应物与生成物,进而书写出反应的表达式,判断反应的类型据此回答问题即可。由于四种物质中W和氧气质量减小,所以是反应物,且反应物的总质量是23g+(64g﹣16g)=71g,而水的质量增加,且增加值是32g﹣5g=27g,依据质量守恒定律参加化学反应的各物质质量总和等于反应后生成的各物质质量总和,所以二氧化碳必是生成物且生成的质量是71g﹣27g=44g;此反应的表达式可表示为W+O2→CO2+H2O。A、由以上分析知X的值等于44g+8g=52g,故错误;B、由于该反应的表达式是W+O2→CO2+H2O,生成物是两种化合物,不属于置换反应,故错误;C、根据质量守恒定律,由反应表达式可以看出W中一定含有碳氢两种元素,是否含有氧元素则要通过生成物中的氧元素与反应的氧气质量进行比较,生成的水中氧元素的质量为:27g×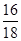 =24g,二氧化碳中氧元素的质量:44g×
=24g,二氧化碳中氧元素的质量:44g×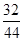 =32g,两者的质量和为56g,而参加反应的氧气的质量=64g﹣16g=48g,所以可判断W中含有氧元素,故错误;D、由C的分析可知W中碳、氢元素质量比为(44g﹣32g):(27g﹣24g)=4:1,故正确,故选D。
=32g,两者的质量和为56g,而参加反应的氧气的质量=64g﹣16g=48g,所以可判断W中含有氧元素,故错误;D、由C的分析可知W中碳、氢元素质量比为(44g﹣32g):(27g﹣24g)=4:1,故正确,故选D。
考点:考查量守恒定律及其应用

下列化学方程式不正确的是
A.细铁丝在氧气中燃烧:3Fe +2O2 Fe3O4 Fe3O4 |
| B.铁丝与硫酸铜溶液反应:Fe+CuSO4=Cu+FeSO4 |
C.碳不完全燃烧:2C+O2 2CO 2CO |
D.用赤铁矿石(主要成分:Fe2O3)炼铁:CO+Fe2O3 2Fe+CO2 2Fe+CO2 |
下列实验装置不能用来证明质量守恒定律的是( )
A. | B. | C. | D. |
C3N4是一种新型材料,它的硬度比金刚石还高,可做切割工具,在C3N4中,C的化合价为+4,则N的化合价是
| A.+5 | B.+3 | C.+1 | D.﹣3 |
吸入氧化镉(CdO)的烟雾可产生急性镉中毒,氧化镉中镉元素的化合价是
| A.+1 | B.﹣1 | C.+2 | D.﹣2 |
铈是一种稀土元素,在元素周期表中铈元素的某些信息如图所示,下列有关铈的说法正确的是
| A.元素符号为Ce | B.属于非金属元素 |
| C.相对原子质量140.1g | D.原子核内中子数位58 |
下列反应属于置换反应的是( )
A.CH4+2O2 CO2+2H2O CO2+2H2O |
B.Fe2O3+3CO 2Fe+3CO2 2Fe+3CO2 |
| C.CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 |
D.C+2CuO 2Cu+CO2↑ 2Cu+CO2↑ |
NH4ClO4(高氯酸铵)可用作火箭推进剂,当它发生分解反应时,不能生成的物质是( )
| A.CO2 | B.Cl2 | C.O2 | D.N2 |