题目内容
通过实验对草酸(相对分子质量是90)进行如下研究。
【查阅资料】①浓硫酸常作干燥剂 ②浓NaOH溶液常用于吸收CO2气体
③无水硫酸铜吸水后由白色变为蓝色 ④氯化钯(PdCl2)溶液遇CO产生黑色沉淀
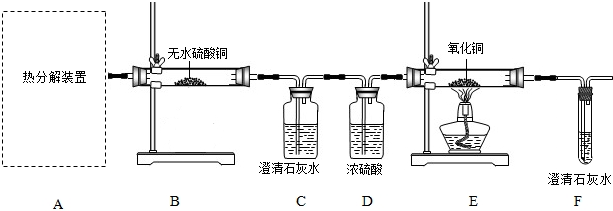
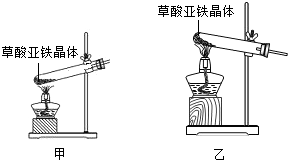
【实验准备】选用下列实验装置(气密性良好,部分固定装置已略去):
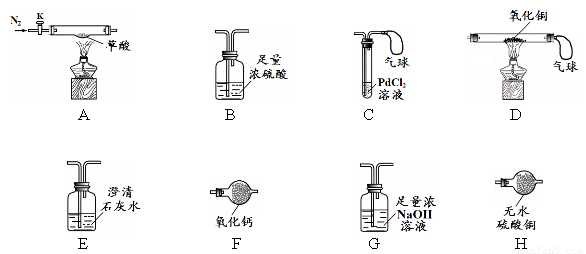
【实验I】检验草酸分解的产物。
|
实验步骤 |
实验现象 |
实验结论及分析 |
|
(1)按A→H→E→C 连接仪器 (2)关闭K,点燃A处酒精灯 |
H中 E中澄清石灰水变浑浊 C中产生黑色沉淀,气球鼓起 |
草酸分解生成了CO2、CO和H2O ①E中反应的化学方程式是 ②C中气球的作用是 |
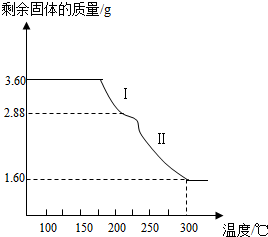
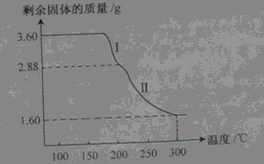
【实验II】取9 g草酸进行实验,测定生成物的质量并确定草酸的组成。
|
实验步骤 |
实验数据 |
实验结论及分析 |
|
(1)选择A、B、D、G装置组合进行实验 (2)鼓入过量的N2后,分别称量B、D、G的质量 (3)关闭K,点燃A、D处的酒精灯,至草酸完全分解 (4)熄灭A处酒精灯,通入过量的N2,熄灭D处酒精灯,再次分别称量B、D、G的质量 |
B装置增重1.8 g D装置中固体质量减少0.8 g G装置增重4.4 g
|
①A、B、D、G装置的正确连接顺序是A→ → →D ②向A中两次通入N2,其中 第二次的目的是 ③草酸的化学式是 ④反思:若用F代替B,则不能测定草酸的组成,其原因是 |
【实验I】 白色固体变成蓝色 ①CO2 +Ca(OH)2 =CaCO3↓+ H20 ②收集尾气(或尾气处理装置)【实验II】①B→G②将生成的气体完全排入吸收装置,使其被完全吸收③C2H2O4 ④CaO可同时吸收H2O、CO2,导致无法准确测量H2O、CO2的质量
【解析】
试题分析:【实验I】根据实验结论由一氧化碳、二氧化碳和水生成,故看到H干燥管中的硫酸铜由白色变为蓝色;①E中所称药品为氢氧化钙水溶液,故反应的化学方程式是CO2 +Ca(OH)2 =CaCO3↓+ H20 ,②C中气球的作用是收集尾气;【实验II】①A、B、D、G装置的正确连接顺序是A→B → G →D; ②向A中两次通入N2,第一次为了排尽装置内的空气,防止发生爆炸,其中第二次的目的是将生成的气体完全排入吸收装置,使其被完全吸收;
③根据装置质量的变化知道生成水1.8g,一氧化碳得到0.8g氧,生成二氧化碳的质量为4.4g,氢元素的质量为:1.8g×2/18×100%=0.2g;
设草酸分解生成一氧化碳的质量为x,
CO+ CuO Cu
+ CO2
Cu
+ CO2
16
x 0.8g
28:16=x:0.8g
x=1.4g
G吸收二氧化碳共4.4g,所以草酸分解生成的二氧化碳的质量为4.4g
分解的草酸的质量为:4.4g+1.4g+1.8g=7.6g,5.4g草酸中碳元素的质量为1.4g×12/28+4.4g×12/44=0.6g+1.2g=1.8g,所以分解的草酸中氧元素的质量为5.4g-1.2g-0.2g=4g,所以草酸中碳、氢、氧元素的质量比为1.2g:0.2g:4g=6:1:20,设草酸的化学式为CxHyOz则
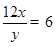 ,
,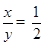 ;
;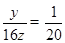 ,
,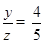
草酸的化学式为C2H2O4
④反思:若用F代替B,则不能测定草酸的组成,其原因是CaO可同时吸收H2O、CO2,导致无法准确测量H2O、CO2的质量
考点:物质的组成

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案通过实验对草酸(相对分子质量是90)进行如下研究。
【查阅资料】①浓硫酸常作干燥剂 ②浓NaOH溶液常用于吸收CO2气体
③无水硫酸铜吸水后由白色变为蓝色 ④氯化 钯(PdCl2)溶液遇CO产生黑色沉淀
钯(PdCl2)溶液遇CO产生黑色沉淀
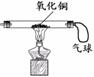
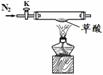
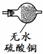
【实验准备】选用下列实验装置(气密性良好,部分固定装置已略去):
 | |||||||
 | |||||||
 |  | ||||||
A B C D
 | |||||||
 | |||||||
 | |||||||
 | |||||||
E F G H
【实验I】检验草酸分解的产物。
| 实验步骤 | 实验现象 | 实验结论及分析 |
| (1)按A→H→E→C 连接仪器 (2)关闭K,点燃A处酒精灯 | H中 E中澄清石灰水变浑浊 C中产生黑色沉淀,气球鼓起 | 草酸分解生成了CO2、CO和H2O ①E中反应的化学方程式是 ②C中气球的作用是 |
【实验II】取9 g草酸进行实验,测定生成物的质量并确定草酸的组成。
| 实验步骤 | 实验数据 | 实验结论及分析 |
| (1)选择A、B、D、G装置组合进行实验 (2)鼓入过量的N2后,分别称量B、D、G的质量 (3)关闭K,点燃A、D处的酒精灯,至草酸完全分解 (4)熄灭A处酒精灯,通入过量的N2,熄灭D处酒精灯,再次分别称量B、D、G的质量 | B装置增重1.8 g D装置中固体 质量减少0.8 g G装置增重4.4 g | ①A、B、D、G装置的正确连接顺序是A→ → →D ②向A中两次通入N2,其中 第二次的目的是 ③草酸的化学式是 ④反思:若用F代替B,则不能测定草酸的组成,其原因是
|