题目内容
在室温下,将Mg、Fe、Al三种金属分别投入足量且质量相等,溶液中溶质的质量分数也相等的硫酸中,反应结束后溶液的质量仍相等,则投入的Mg、Fe、Al三种金属质量关系是
- A.Mg>Al>Fe
- B.Fe>Mg>Al
- C.Al>Mg>Fe
- D.Mg=Al=Fe
C
分析:将Mg、Fe、Al三种金属分别投入足量且质量相等,溶液中溶质的质量分数也相等的硫酸中,反应结束后溶液的质量仍相等,说明溶液质量增加的质量相等,即加入的金属质量减去生成的氢气的质量相等来考虑本题.
解答:在没加入金属前溶液是硫酸溶液,质量相等,溶液中溶质的质量分数也相等,加入金属后反应结束溶液的质量仍相等,说明烧杯内溶液的增加量相同,即加入金属的质量-生成氢气的质量相等,设铝的质量为X,镁得质量为Y,铁的质量为Z,则X-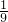 X=Y-
X=Y-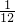 Y=Z-
Y=Z-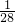 Z即:
Z即: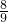 X=
X= Y=
Y=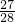 Z,所以X>Y>Z即:Al>Mg>Fe.
Z,所以X>Y>Z即:Al>Mg>Fe.
故选C.
点评:解答本题的关键是要知道反应结束后溶液的质量仍相等,说明溶液质量增加的质量相等,即加入的金属质量减去生成的氢气的质量相等.
分析:将Mg、Fe、Al三种金属分别投入足量且质量相等,溶液中溶质的质量分数也相等的硫酸中,反应结束后溶液的质量仍相等,说明溶液质量增加的质量相等,即加入的金属质量减去生成的氢气的质量相等来考虑本题.
解答:在没加入金属前溶液是硫酸溶液,质量相等,溶液中溶质的质量分数也相等,加入金属后反应结束溶液的质量仍相等,说明烧杯内溶液的增加量相同,即加入金属的质量-生成氢气的质量相等,设铝的质量为X,镁得质量为Y,铁的质量为Z,则X-
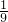 X=Y-
X=Y-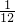 Y=Z-
Y=Z-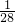 Z即:
Z即: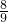 X=
X= Y=
Y=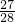 Z,所以X>Y>Z即:Al>Mg>Fe.
Z,所以X>Y>Z即:Al>Mg>Fe.故选C.
点评:解答本题的关键是要知道反应结束后溶液的质量仍相等,说明溶液质量增加的质量相等,即加入的金属质量减去生成的氢气的质量相等.

练习册系列答案
相关题目