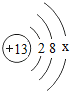��Ŀ����
����Ŀ��(3��) 2009�������������ڵ������籾�������С��й���ŵ����2020�굥λ����������ֵ���ŷŵĶ�����̼��2005���½�40����45����
��������ѧ���������ڼ��ٴ����ж�����̼�������о���
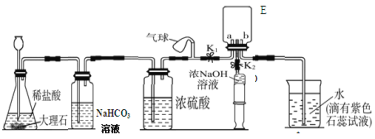
���������е�CO2ѹ���������ڱ����������п�ѧ�ҵ��������������Ӻ�ˮ����ȣ����º�������������CO2ʹ��ˮ������ӵ�ԭ����_________________��(�û�ѧ����ʽ��ʾ)��
���������CO2�������ڴ����ͼ��ȵ������·�Ӧ��ת��Ϊˮ�ͼ��顣�����Ӧ�Ļ�ѧ����ʽ��__________________________________��
������δ�����������Դ��ʵ������ȡ������ԭ��Ϊ__________________________��
���𰸡� ��1�� CO2 + H2O = H2CO3 ��2�� CO2 + 4H2![]() CH4 + 2H2O ��3�� Zn + H2SO4 = ZnSO4 + H2��
CH4 + 2H2O ��3�� Zn + H2SO4 = ZnSO4 + H2��
��������
�����������1�����������е�CO2ѹ���������ڱ����������п�ѧ�ҵ��������������Ӻ�ˮ����ȣ����º�������������CO2ʹ��ˮ������ӵ�ԭ����CO2 + H2O = H2CO3 ���������CO2�������ڴ����ͼ��ȵ������·�Ӧ��ת��Ϊˮ�ͼ��顣�����Ӧ�Ļ�ѧ����ʽ��CO2 + 4H2![]() CH4 + 2H2O����2��������δ�����������Դ��ʵ������ȡ������ԭ��ΪZn + H2SO4 = ZnSO4 + H2����
CH4 + 2H2O����2��������δ�����������Դ��ʵ������ȡ������ԭ��ΪZn + H2SO4 = ZnSO4 + H2����

����Ŀ��ά����C������ˮ��ˮ��Һ�����ԣ��ױ���������������ijͬѧΪ��̽��VC�����ʣ�����������ʵ��.
������ij��ҩ��������VCƬ��ÿƬ��VC0.1g�������Ը��ϣ�����0.5%��VC��Һ��
��1����ȡ5ƬVCƬ��Ӧ��Լȥ����ˮ mL.(ȡ����)
��2����ȥ����Һ�еIJ����Ը��ϣ��õ������VC��Һ������������� ��
�������ʵ��֤��VC��Һ�������ԡ�
��3�������Լ�����ɫ��̪��Һ��ϡ����������Һ����������±���
ʵ�鲽�� | Ԥ�������� |
| ��˵��VC��Һ�������� |
����̽��VC��Һ��һ���¶��£�18����¶��ʱ���VC������Ӱ�죬���ÿ��Ʊ������������飬�������±���ʾ��
ʵ����� | ��ˮŨ�ȼ����� | 0.6%������Һ | VC��Һ����¶��ʱ��/h | ��ɫ��ʧ��ҪVC��Һ���� |
�� | 0.06%��4.8mL | 3�� | 0 | 10 |
�� | 0.06%��4.8mL | 3�� | 12 | 12 |
�� | 3�� | 24 | 18 | |
�� | 0.06%��4.8mL | 3�� | 36 | 41 |
��4��ʵ�����е�ˮ��Ũ�ȼ������ֱ��� ��
��5��VC����������¶��ʱ�䣨0����36h���ı仯ͼ����ȷ���� ������ĸ��ţ�
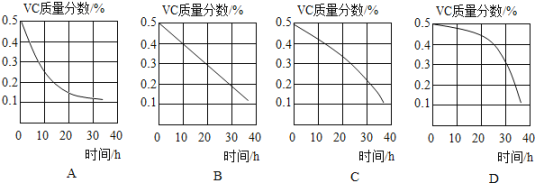
��6��Ϊ����߶���̽��vc��Һ��ȷ�ԡ�����VC��Һʱ�������ȳ�ȥ�ܽ�������ˮ�е��������������崦�������� ��