题目内容
【题目】为了测定样品CaSO4XH2O和CaCO3混合物的组成,实验小组利用下图所示的装置(夹持仪器省略)进行实验。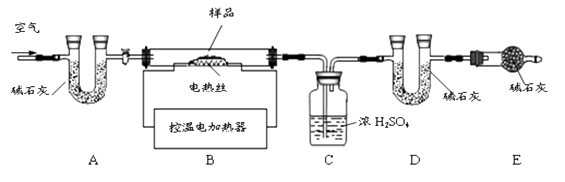
(1)实验前首先要 , 再装入样品。装置A中碱石灰的作用是。
(2)C装置的作用是应用了浓硫酸具有的性质。
(3)已知CaSO4XH2O失去全部结晶水的温度为160℃,1350℃时CaSO4开始分解;CaCO3在900℃时分解完全。现控制B装置温度900℃进行实验,并采集了如下实验数据:
a.样品的质量为m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g
若实验测得m1=22.20 g,m3=3.60 g,m4=2.20 g。
求:①样品中CaCO3的质量 g;②X的值。
(4)装置E的作用是 , 若缺少E装置,测得CaCO3的质量(选填“偏大”、“偏小”、“不变”),X的值会(选填“偏大”、“偏小”、“不变”)。
(5)你认为还可选用下列(选填序号)数据组合也可求出X的值。
A.ab
B.abd
C.bcd
(6)CaSO4当温度达到1350℃时分解会产生一种固体氧化物与两种气体,其中一种气体有刺激性气味,其分解的化学方程式为。
【答案】
(1)检查装置气密性,除去鼓入空气中二氧化碳和水蒸气
(2)吸水性
(3)5,2
(4)防止空气中二氧化碳和水蒸气进入装置D中,偏大,偏大
(5)B,C
(6)2CaSO4 ![]() 2 CaO+2SO2↑+O2↑
2 CaO+2SO2↑+O2↑
【解析】根据所学知识和题中信息知,(1)实验前首先要检查装置气密性,再装入样品。装置A中碱石灰的作用是除去鼓入空气中二氧化碳和水蒸气。(2)C装置的作用是应用了浓硫酸具有吸水性的性质。(3)①样品中CaCO3的质量是CaCO3→CO2, ![]() =
= ![]() ,x=5g.②X的值是CaSO4XH2O→XH2O,
,x=5g.②X的值是CaSO4XH2O→XH2O, ![]() =
= ![]() ,x=2. (4)装置E的作用是防止空气中二氧化碳和水蒸气进入装置D中. 若缺少E装置,测得CaCO3的质量偏大。X的值会偏大。(5)下列B.abd 或 C.bcd 数据组合也可求出X的值。(6)CaSO4当温度达到1350℃时分解会产生一种固体氧化物与两种气体,其中一种气体有刺激性气味,其分解的化学方程式为2CaSO4
,x=2. (4)装置E的作用是防止空气中二氧化碳和水蒸气进入装置D中. 若缺少E装置,测得CaCO3的质量偏大。X的值会偏大。(5)下列B.abd 或 C.bcd 数据组合也可求出X的值。(6)CaSO4当温度达到1350℃时分解会产生一种固体氧化物与两种气体,其中一种气体有刺激性气味,其分解的化学方程式为2CaSO4 ![]() 2 CaO+2SO2↑+O2↑。
2 CaO+2SO2↑+O2↑。
所以答案是:检查制作气密性、除去鼓入空气中二氧化碳和水蒸气、吸水性、5 、2、防止空气中二氧化碳和水蒸气进入装置D中、偏大、偏大、BC、
2CaSO4 ![]() 2 CaO+2SO2↑+O2↑。
2 CaO+2SO2↑+O2↑。

【题目】下列各选项中,解释与事实不吻合的是
选项 | 事实 | 解释 |
A | 打开汽水瓶盖时,汽水自动喷出 | 气体的溶解度随压强的减小而减小 |
B | 充气的篮球有弹性 | 分子间有间隔 |
C | 金刚石很坚硬,而石墨却很软 | 碳原子的排列方式不同 |
D | 酒精做温度计的填充物 | 酒精分子的体积大小随温度升降而改变 |
A.AB.BC.CD.D