题目内容
(2012?桂平市三模)在开展复分解反应研究性学习中,某学习小组设计了如下学习思路: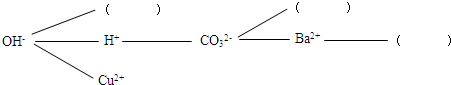
[练习总结]下列各组物质间均能发生反应,请写出③发生反应的化学方程式.
①稀盐酸与氢氧化钠溶液;②碳酸钠溶液与稀硫酸;
③碳酸钠溶液与氯化钡溶液
[探究讨论]上述反应为什么能够发生?这是因为这些反应物中含有特殊的阴、阳离子,如①中有H+和OH-,②中有H+和CO32-,③中有
[构建网络]按照一定的顺序排列这些离子,就可以形成一种网络形式.在网络中,用短线相连的这些阴、阳离子能两两结合生成沉淀或气体或水.现有Ca2+、SO42-、NH4+,请将它们填入下面合适的“
[反思拓展](1 )通过形成的网络,可以判断化合物间能否共存、进行物质的鉴别、用于物质的除杂等.氯化钠中混有碳酸钠,可以加入
(2)请举出一组由盐和碱组成的能发生复分解反应的溶液组:
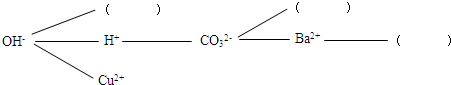
[练习总结]下列各组物质间均能发生反应,请写出③发生反应的化学方程式.
①稀盐酸与氢氧化钠溶液;②碳酸钠溶液与稀硫酸;
③碳酸钠溶液与氯化钡溶液
BaCl2+Na2CO3=BaCO3↓+2NaCl
BaCl2+Na2CO3=BaCO3↓+2NaCl
.[探究讨论]上述反应为什么能够发生?这是因为这些反应物中含有特殊的阴、阳离子,如①中有H+和OH-,②中有H+和CO32-,③中有
Ba2+和CO32-
Ba2+和CO32-
.[构建网络]按照一定的顺序排列这些离子,就可以形成一种网络形式.在网络中,用短线相连的这些阴、阳离子能两两结合生成沉淀或气体或水.现有Ca2+、SO42-、NH4+,请将它们填入下面合适的“
NH4+;Ca2+;SO42-
NH4+;Ca2+;SO42-
”中,使其形成一个更为完整的复分解反应的网络.[反思拓展](1 )通过形成的网络,可以判断化合物间能否共存、进行物质的鉴别、用于物质的除杂等.氯化钠中混有碳酸钠,可以加入
氯化钙
氯化钙
(填写化学名称)除去碳酸钠(2)请举出一组由盐和碱组成的能发生复分解反应的溶液组:
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
.分析:运用酸碱盐的知识解决该题,根据复分解反应的条件生成沉淀或气体或生成水复分解反应才能发生填空,最后复分解反应网络用Ca2+、SO42-、NH4+的特性解决.
解答:解:【练习总结】碳酸钠溶液和氯化钡溶液反应生成碳酸钡和氯化钠,故③答案:BaCl2+Na2CO3=BaCO3↓+2NaCl;
【探究讨论】阴、阳离子能两两结合生成沉淀或气体或水,复分解反应就可发生,③中Ba2+和CO32-生成沉淀,故答案为:③Ba2+和CO32-;
【构建网络】在这三种离子中NH4+与OH-能产生氨气和水,钙离子能与碳酸根离子产生白色沉淀,钡离子能与硫酸根离子产生白色沉淀,故答案:NH4+;Ca2+;SO42-;
【反思拓展】(1)除去氯化钠中的碳酸钠实际是除去碳酸根离子,由题中复分解反应网络知选用钙盐,又不能引入新杂质所以选氯化钙,
故答案:氯化钙
(2)氯化镁和氢氧化钠的反应属于盐和碱的反应,符号复分解反应的条件,反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl
故答案为:【练习总结】BaCl2+Na2CO3=BaCO3↓+2NaCl;
【探究讨论】:③Ba2+和CO32-;
【构建网络】NH4+;Ca2+;SO42-;
【反思拓展】(1)氯化钙;(2)MgCl2+2NaOH=Mg(OH)2↓+2NaCl
【探究讨论】阴、阳离子能两两结合生成沉淀或气体或水,复分解反应就可发生,③中Ba2+和CO32-生成沉淀,故答案为:③Ba2+和CO32-;
【构建网络】在这三种离子中NH4+与OH-能产生氨气和水,钙离子能与碳酸根离子产生白色沉淀,钡离子能与硫酸根离子产生白色沉淀,故答案:NH4+;Ca2+;SO42-;
【反思拓展】(1)除去氯化钠中的碳酸钠实际是除去碳酸根离子,由题中复分解反应网络知选用钙盐,又不能引入新杂质所以选氯化钙,
故答案:氯化钙
(2)氯化镁和氢氧化钠的反应属于盐和碱的反应,符号复分解反应的条件,反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl
故答案为:【练习总结】BaCl2+Na2CO3=BaCO3↓+2NaCl;
【探究讨论】:③Ba2+和CO32-;
【构建网络】NH4+;Ca2+;SO42-;
【反思拓展】(1)氯化钙;(2)MgCl2+2NaOH=Mg(OH)2↓+2NaCl
点评:本题在对复分解反应发生的条件分析的基础上对化学反应进行了考查并且延伸到物质鉴别,综合性强.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目