题目内容
17.根据图1所示实验装置回答问题: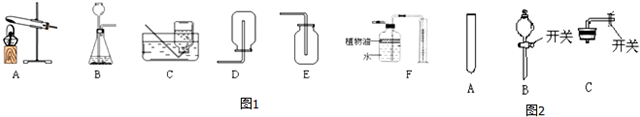
(1)小明同学选择A装置准备用高锰酸钾为原料制取一瓶纯净的氧气(不考虑水蒸气),他应选择的收集装置是C(填字母),写出该方法制取氧气的化学反应方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)小华同学想用过氧化氢溶液和二氧化锰为原料代替高锰酸钾制取一瓶氧气,她选择的发生装置是B(填字母),理由过氧化氢溶液和二氧化锰为原料制氧气,是固体与液体在常温下反应.
(3)当过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速度和生成氧气的量.如果你稍改变选择装置,便可控制其反应速度,请从图2的仪器中选择一种仪器更换小华同学选择的装置中一种仪器,以达到控制反应速度的目的,你选择的仪器是B(填序号),它更换原装置中的长颈漏斗 (填名称).你认为以上小明和小华制取氧气的方法中哪一种更好,小华,理由是小华用过氧化氢溶液制氧气不需要加热,装置还可以随时添加药品从而控制生成气体的质量,节约药品.改装后的装置可以制取乙炔(C2H2)气体;乙炔是用CaC2和水反应制取.请完成制取乙炔的化学方程式CaC2+2H2O═Ca(OH)2+C2H2↑.
(4)若实验室对你开放,选用B和E装置还可制取二氧化碳气体,你还需向实验老师领取的药品有大理石(或石灰石)、稀盐酸(写名称),其反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
F装置可用来测量生成的这种气体的体积,其中在水面上放一层植物油的目的是防止二氧化碳溶于水;植物油上方原有的空气对实验的结果没有(填“有”或“没有”)明显影响.
分析 (1)收集纯净的气体通常用排水法,并据反应原理书写方程式;
(2)要根据药品的状态和反应条件选择的发生装置;
(3)要控制其反应速度,选择的加入药品的仪器,要能控制加入的量及速率,才能达到目的;利用过氧化氢溶液制取氧气不需加热,且还可以随时添加药品从而控制生成氧气的量,节约药品;并利用反应物和生成物及质量守恒定律,书写实验室制取乙炔的化学方程式;
(4)B装置属于固液常温型,E收集密度比空气大的气体,所以该套装置还可用来制取二氧化碳,所用药品是大理石或石灰石和稀盐酸,据反应原理书写方程式,二氧化碳气体能溶于水,不溶于油,可推出在水面上放一层植物油的目的防止CO2与水接触.
解答 解:(1)氧气是难溶于水,密度比空气大的气体,可以用排水法和向上排空气法收集,排水法收集的气体较纯,排空气法收集的气体干燥,故应选择的收集装置是C,高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)过氧化氢溶液和二氧化锰为原料制氧气,是固体与液体在常温下反应,用发生装置B;
(3)分液漏斗可以控制加入液体药品的量和速率,所以用B(分液漏斗)来代替原装置中的长颈漏斗;小华制氧气的装置较好,因为小华用过氧化氢溶液制氧气不需要加热,节约能源,装置还可以随时添加药品从而控制生成氧气的质量,节约药品;用改装后的装置制取乙炔气体,利用反应物和生成物及质量守恒定律,反应前后元素的种类、原子的数目不变,写出乙炔制取的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑;
(4)装置B为固液不加热装置,装置E是采用向上排空气法收集,可以选用这两个装置制取的气体除了氧气还有二氧化碳,实验室用大理石与稀盐酸来制取二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;要测量二氧化碳的体积只能用排水法,用量筒测量水的体积从而测二氧化碳的体积,二氧化碳能溶于水,所以要在水的上方放一层植物油,油上方的空气对实验结果没有影响;
故答案为:
(1)C;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)B;过氧化氢溶液和二氧化锰为原料制氧气,是固体与液体在常温下反应;
(3)B;长颈漏斗;小华;小华用过氧化氢溶液制氧气不需要加热,装置还可以随时添加药品从而控制生成气体的质量,节约药品;
CaC2+2H2O=Ca(OH)2+C2H2↑;
(4)二氧化碳;大理石(或石灰石)、稀盐酸;CaCO3+2HCl=CaCl2+H2O+CO2↑;防止二氧化碳溶于水;没有.
点评 化学是一门以实验为基础的学科,因此实验仪器的使用、气密性的检查、实验现象的描述、装置的选择及注意事项,以及气体的制取和检验,都将是中考热点;另外,装置的评价可以考查学生的思维能力,创新能力,中考中尤为突出.

 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案| A. | 农夫山泉 | B. | 伊利纯牛奶 | C. | 蒸馏水 | D. | 雪花啤酒 |
 新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.
新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.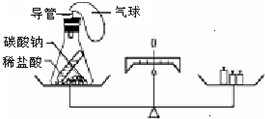 某同学用图装置探究质量守恒定律.
某同学用图装置探究质量守恒定律.