题目内容
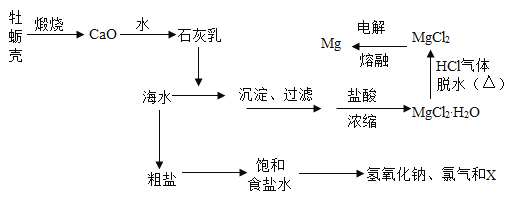
【题目】以天然气(含少量 H2S 气体)为原料可获得工业合成氨所需的 N2 和 H2,其转化步骤如下:
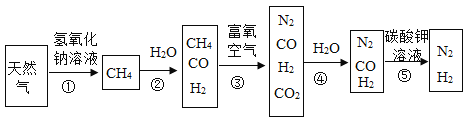
(1)天然气属于____燃料。合成氨的反应方程式为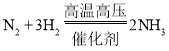 ,该反应属于_________(填基本反应类型)。氨气(NH3)常用于制备__________(填“氮”、“磷”或“钾”)肥。
,该反应属于_________(填基本反应类型)。氨气(NH3)常用于制备__________(填“氮”、“磷”或“钾”)肥。
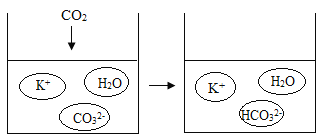
(2)步骤⑤中所涉化学反应前后主要微粒种类变化如图所示。试写出该反应的化学方程式:_______。
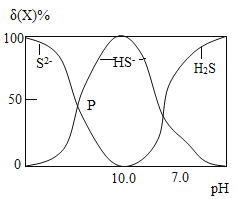
(3)步骤①中所用NaOH 溶液可吸收天然气中的H2S 气体并与之发生反应。常温下随着 H2S不断被吸收,NaOH 溶液的pH逐渐减小,溶液中含硫粒子(S2-、HS-、H2S)的分布δ(X)如图所示。
注:已知H2S气体溶于水后可解离出H+、HS-和 S2-。
δ(X)=![]()
①溶液的 pH=7 时,溶液呈________(填“酸性”、“碱性”或“中性”)。P 点对应的溶液中溶质主要为NaHS 和________,溶液中 S2-的个数_________(填“大于”、“等于”或“小于”)HS-的个数。
②当溶液的 pH=10 时,NaOH 与H2S 反应的化学方程式为____________。
【答案】化石 化合 氮 CO2+K2CO3+H2O=2KHCO3 中性 Na2S 等于 NaOH+H2S=NaHS+H2O
【解析】
(1)煤、石油和天然气常称为化石燃料;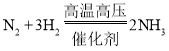 ,是多变一的反应类型,符合化合反应类型;氨气(NH3)中含有的是氮元素,所以它常用来制备氮肥。故填:化石;化合;氮。
,是多变一的反应类型,符合化合反应类型;氨气(NH3)中含有的是氮元素,所以它常用来制备氮肥。故填:化石;化合;氮。
(2)根据反应的微粒种类变化图可知二氧化碳和碳酸钾、水反应生成碳酸氢钾,反应的化学方程式为:CO2+K2CO3+H2O=2KHCO3,故填:CO2+K2CO3+H2O=2KHCO3。
(3)①pH 的范围通常在014之间。pH小于7的溶液呈酸性,pH等于7的溶液呈中性,pH大于7的溶液呈碱性;又图像可知P点的时候是S2-、HS-的含量的交点,代表这两种物质都存在溶液中且含硫离子的个数相同,所以P 点对应的溶液中溶质主要为NaHS 和Na2S。故填:中性;Na2S;等于。
②当溶液的 pH=10 时,由图像可知溶液中只存在HS-,所以NaOH与H2S反应在此时只生成NaHS和水,反应的化学方程式为:NaOH+H2S=NaHS+H2O;故填:NaOH+H2S=NaHS+H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案