题目内容
工业上,高温煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳.如果高温煅烧含碳酸钙80%的石灰石25 t(杂质不反应),最多可制得二氧化碳多少吨?
解:设生成二氧化碳的质量为x.
CaCO3 CaO+CO2↑
CaO+CO2↑
100 44
25t×80% x
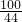 =
=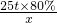 ,x=8.8t
,x=8.8t
答:最多可制得二氧化碳8.8t.
分析:由石灰石的质量和含碳酸钙的质量分数可以根据碳酸钙高温分解的化学方程式计算出生成二氧化碳的质量.
点评:本题主要考查含杂质物质的化学方程式计算,难度稍大.
CaCO3
 CaO+CO2↑
CaO+CO2↑100 44
25t×80% x
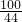 =
=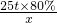 ,x=8.8t
,x=8.8t答:最多可制得二氧化碳8.8t.
分析:由石灰石的质量和含碳酸钙的质量分数可以根据碳酸钙高温分解的化学方程式计算出生成二氧化碳的质量.
点评:本题主要考查含杂质物质的化学方程式计算,难度稍大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
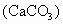 可制得生石灰和二氧化碳.如果要制取5.6t氧化钙,需要碳酸钙多少吨?
可制得生石灰和二氧化碳.如果要制取5.6t氧化钙,需要碳酸钙多少吨?