题目内容
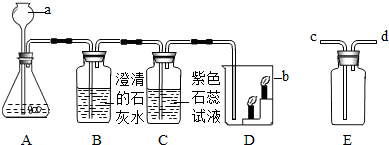
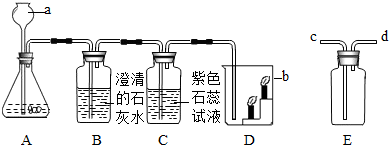
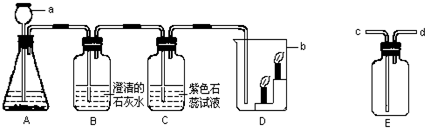
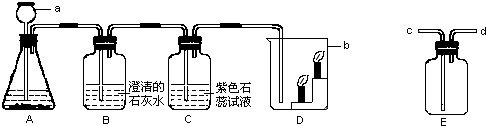
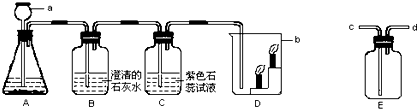
如图是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质的实验装置图,试根据题目要求回答下列问题:
(1)写出装置A中发生的化学方程式.
(2)装置C中观察到的现象是什么?
(3)装置D中观察到下层蜡烛先熄灭,上层蜡烛后熄灭,此实验现象说明二氧化碳具有哪些性质?
(4)实验室用装置E来收集二氧化碳时,二氧化碳应从哪些端(填“c端”或“d端”)通入?

(1)写出装置A中发生的化学方程式.
(2)装置C中观察到的现象是什么?
(3)装置D中观察到下层蜡烛先熄灭,上层蜡烛后熄灭,此实验现象说明二氧化碳具有哪些性质?
(4)实验室用装置E来收集二氧化碳时,二氧化碳应从哪些端(填“c端”或“d端”)通入?
分析:(1)熟悉、识记实验室用碳酸钙与稀盐酸反应制取二氧化碳的化学反应式的书写;
(2)考虑二氧化碳与水反应;
(3)根据提供的信息和二氧化碳的性质解决问题;
(4)根据二氧化碳的密度大于空气的密度来确定进气端.
(2)考虑二氧化碳与水反应;
(3)根据提供的信息和二氧化碳的性质解决问题;
(4)根据二氧化碳的密度大于空气的密度来确定进气端.
解答:解:(1)图A中是碳酸钙与稀盐酸,化学反应式是:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)二氧化碳与水反应生成碳酸,碳酸使紫色石蕊试液遇酸变红,所以C中的现象是:紫色的石蕊试液变红;
(2)根据提供的信息:装置D中观察到下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳的密度比空气大,它不能燃烧,也不能支持燃烧.说明二氧化碳可用于灭火.
(4)二氧化碳的密度大于空气的密度,用E装置收集二氧化碳时,可从c端进,以排净瓶底的空气.
故答案为:(1)CaCO3+2HCl=CaCl2+CO2↑+H2O;(2)紫色的石蕊试液变红
(3)二氧化碳的密度比空气大,它不能燃烧,也不能支持燃烧.(4)c端水
(2)二氧化碳与水反应生成碳酸,碳酸使紫色石蕊试液遇酸变红,所以C中的现象是:紫色的石蕊试液变红;
(2)根据提供的信息:装置D中观察到下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳的密度比空气大,它不能燃烧,也不能支持燃烧.说明二氧化碳可用于灭火.
(4)二氧化碳的密度大于空气的密度,用E装置收集二氧化碳时,可从c端进,以排净瓶底的空气.
故答案为:(1)CaCO3+2HCl=CaCl2+CO2↑+H2O;(2)紫色的石蕊试液变红
(3)二氧化碳的密度比空气大,它不能燃烧,也不能支持燃烧.(4)c端水
点评:本题以实验探究的形式考查二氧化碳的灭火性、与水的反应、密度等特点,属于基础知识类题目,较好做.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目