题目内容
某实验小组开展了如下有关碱的化学性质探究活动:
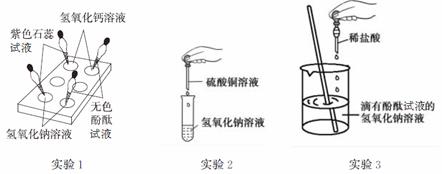
(1)实验1的目的是 。
(2)实验2中发生反应的化学方程 式是 。
式是 。
(3)实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。小萍加入的试剂可能是 。
(4)通过上述实验探究活动,可以总结出碱的化学性质是:
①碱能与酸发生中和反应;
② ;
······
(5)准备实验时,小英发现药品室有两瓶未标注浓度的氢氧化钠溶液,经询问老师得知,这两瓶溶液的溶质质量分数分别为 5%和10%。请你设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸)。
5%和10%。请你设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸)。
| 实验步骤 | 预计现象及相应结论 |
| _____________________________________ _____________________________________ _____________________________________ | _________________________________________为5%的氢氧化钠溶液,另一种为10%的氢氧化钠溶液 |
(1)探究碱与指示剂作用 (2)CuSO4+2NaOH Cu(OH)2↓+Na2SO4 (3)紫色石蕊试液(或锌等活泼金属,碳酸钠溶液,氢氧化钠溶液等,写化学
Cu(OH)2↓+Na2SO4 (3)紫色石蕊试液(或锌等活泼金属,碳酸钠溶液,氢氧化钠溶液等,写化学 式也可) (4)碱能与某些盐反应(或碱能与指示剂反应)
式也可) (4)碱能与某些盐反应(或碱能与指示剂反应)
(5)
| 实验 | 预计现象及相应结论 |
| 取2支洁净的试管,分别加入等体积的两种待测溶液,再分别滴加相同滴数的无色酚酞试液,向溶液中滴加10%的稀盐酸,计算红色刚好消失时所滴加稀盐酸的滴数(或用量) | 红色刚好消失时所滴加稀盐酸的滴数少的一种 |
(其他方案合理也可)
解析:(1)紫色 石蕊试液和无色酚酞试液属于酸碱指示剂,因此实验1探究的是碱与指示剂的作用。(2)硫酸铜溶液和氢氧化钠溶液反应会生成氢氧化铜蓝色沉淀和硫酸钠。(3)溶液由红色变为无色,说明氢氧化钠已经反应完,此时有两种情况:恰好完全反应或盐酸过量,要想判断盐酸是否过量可根据酸的性质设计实验,如:加入紫色石蕊试液变红色,就说明盐酸过量。(4)通过所做实验可总结出碱有以下性质:①碱能与酸发生中和反应,②碱能与指示剂作用,③碱能与某些盐反应。(5)5%的氢氧化钠溶液比10%的氢氧化钠溶液碱性弱,因此取等体积的两种待测液分别与等浓度的稀盐酸恰好完全反应时,5%的氢氧化钠溶液需要的稀盐酸要少,可根据以上分析设计实验,但要注意控制变量法的运用。
石蕊试液和无色酚酞试液属于酸碱指示剂,因此实验1探究的是碱与指示剂的作用。(2)硫酸铜溶液和氢氧化钠溶液反应会生成氢氧化铜蓝色沉淀和硫酸钠。(3)溶液由红色变为无色,说明氢氧化钠已经反应完,此时有两种情况:恰好完全反应或盐酸过量,要想判断盐酸是否过量可根据酸的性质设计实验,如:加入紫色石蕊试液变红色,就说明盐酸过量。(4)通过所做实验可总结出碱有以下性质:①碱能与酸发生中和反应,②碱能与指示剂作用,③碱能与某些盐反应。(5)5%的氢氧化钠溶液比10%的氢氧化钠溶液碱性弱,因此取等体积的两种待测液分别与等浓度的稀盐酸恰好完全反应时,5%的氢氧化钠溶液需要的稀盐酸要少,可根据以上分析设计实验,但要注意控制变量法的运用。

某实验小组开展了如下有关碱的化学性质探究活动:
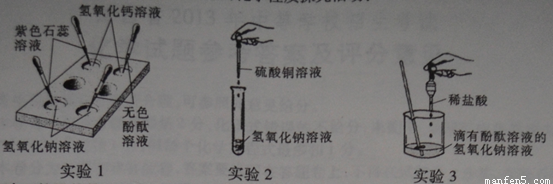
(1)买验l的目的是 ;
(2)实验2中发生反应的化学方程式是 ;
(3)实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含
有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。
小萍加入的试剂可能是 ;
(4)通过上述实验探究活动,可以总结出碱的化学性质是:
①碱能与酸发生中和反应(精校);
② ;
…………
(5)准备实验时,小英发现药品室有两瓶未标注浓度的氢氧化钠溶液,经询问老师得知,该两瓶溶液的溶质质量分数分别为5%和l0%。请你设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸)。
|
实验步骤 |
预计现象及相应结论 |
|
|
为5%的氢氧化钠溶液,另一种为l0%的氢氧化钠溶液。 |