题目内容
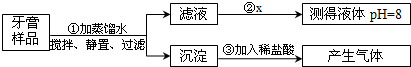
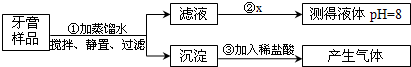
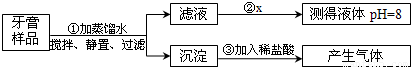
小丽同学按下列流程步骤对某牙膏进行探究.已知牙膏中常用氢氧化铝、碳酸钙等一种或几种物质作摩擦剂.
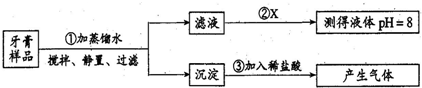
(1)步骤①中所需要的玻璃仪器除了烧杯、玻璃棒外,还需下图仪器中的
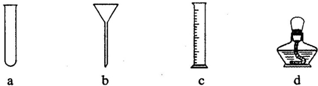
(2)步骤②中小丽选用的x是
A.石蕊溶液 B.酚酞溶液 C.pH试纸
(3)通过探究,你认为牙膏的pH范围比较适宜的是
A.5~6 B.8~9 C.12-13
(4)从步骤③的探究结果看,小丽可验出摩擦剂中一定存在
(5)氢氧化铝具有在酸(如稀硫酸)或碱溶液(如NaOH溶液)中均能发生中和反应而生成盐溶液的性质(两性).为进一步证明Al(OH)3是否存在,可以将过滤所得沉淀加入

(1)步骤①中所需要的玻璃仪器除了烧杯、玻璃棒外,还需下图仪器中的
b
b
,玻璃棒在步骤①中的一种作用是搅拌(或加快溶解或引流)
搅拌(或加快溶解或引流)
.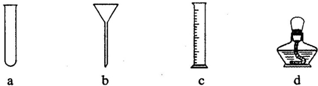
(2)步骤②中小丽选用的x是
C
C
.A.石蕊溶液 B.酚酞溶液 C.pH试纸
(3)通过探究,你认为牙膏的pH范围比较适宜的是
B
B
A.5~6 B.8~9 C.12-13
(4)从步骤③的探究结果看,小丽可验出摩擦剂中一定存在
碳酸钙
碳酸钙
,原因是(用化学方程式表示)CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.(5)氢氧化铝具有在酸(如稀硫酸)或碱溶液(如NaOH溶液)中均能发生中和反应而生成盐溶液的性质(两性).为进一步证明Al(OH)3是否存在,可以将过滤所得沉淀加入
NaOH溶液
NaOH溶液
中,若观察到沉淀部分消失
沉淀部分消失
,即可证明存在氢氧化铝.分析:(1)根据溶解过滤时用到的仪器进行分析,根据过滤操作时玻璃棒的作用进行分析;
(2)根据酸碱指示剂只会指示溶液的酸碱性,不会测出pH值进行分析,
(3)根据测出的pH值进行分析,
(4)根据沉淀会与盐酸反应生成气体,确定含有碳酸钙,
(5)根据氢氧化铝的化学性质进行分析.
(2)根据酸碱指示剂只会指示溶液的酸碱性,不会测出pH值进行分析,
(3)根据测出的pH值进行分析,
(4)根据沉淀会与盐酸反应生成气体,确定含有碳酸钙,
(5)根据氢氧化铝的化学性质进行分析.
解答:解:(1)除了提供的仪器外,在过滤时,该过滤器中还需要有支撑滤纸的装置,图示仪器中漏斗在过滤时,可以起到该作用; 在溶解过程中玻璃棒搅拌可以加速溶解,过滤时,用玻璃棒引流,防止将液体倒在外面,
(2)酸碱指示剂只会指示溶液的酸碱性,不会测出pH值,PH试纸可以测出溶液的酸碱度,因此需要用pH试纸,
(3)各处滤液的pH值是8,所以牙膏显弱碱性,因此选B.
(4)从牙膏的陈分分析可知碳酸钙能和盐酸反应生成氯化钙、水和二氧化碳,其方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)氢氧化铝固体既能与酸反应生成盐溶液和水,也能和碱反应生成盐溶液和水,要证明Al(OH)3的存在,加入的物质不能和碳酸钙反应,只能加入碱,因此加入氢氧化钠的溶液,当发现沉淀部分溶解,即可证明存在氢氧化铝.
故答案为(1)b;搅拌(或加快溶解或引流)(2)C (3)B (4)碳酸钙; CaCO3+2HCl=CaCl2+H2O+CO2↑ (5)NaOH溶液;沉淀部分消失
(2)酸碱指示剂只会指示溶液的酸碱性,不会测出pH值,PH试纸可以测出溶液的酸碱度,因此需要用pH试纸,
(3)各处滤液的pH值是8,所以牙膏显弱碱性,因此选B.
(4)从牙膏的陈分分析可知碳酸钙能和盐酸反应生成氯化钙、水和二氧化碳,其方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)氢氧化铝固体既能与酸反应生成盐溶液和水,也能和碱反应生成盐溶液和水,要证明Al(OH)3的存在,加入的物质不能和碳酸钙反应,只能加入碱,因此加入氢氧化钠的溶液,当发现沉淀部分溶解,即可证明存在氢氧化铝.
故答案为(1)b;搅拌(或加快溶解或引流)(2)C (3)B (4)碳酸钙; CaCO3+2HCl=CaCl2+H2O+CO2↑ (5)NaOH溶液;沉淀部分消失
点评:该题主要考查了过滤和测定溶液的pH值,以及对氢氧化铝的特殊的性质进行了整合考查,需要注意酸碱指示剂只会指示酸碱性,要知道具体的pH值,需要用pH试纸测定.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目