题目内容
如图是A、B、C三种物质的溶解度随温度变化的曲线图.根据图回答:
(1)在甲图中,t3℃时,A、B、C三种物质中,溶解度最大的物质是 .P点所表示的含义为 ;随着温度的升高,A、B、C三种物质的饱和溶液中有溶质从溶液中析出的是 ;
t℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法 、 、 ;
要将B物质从它的饱和溶液中析出,应采用的方法是 (填“冷却”或“蒸发”).
(2)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种? .
(3)丙图中,S表示物质的溶解度,在 ℃时SA=SB>SC;
t3℃时,A物质的饱和溶液中溶质的质量分数为 ,90gA物质的饱和溶液中,含有A物质 g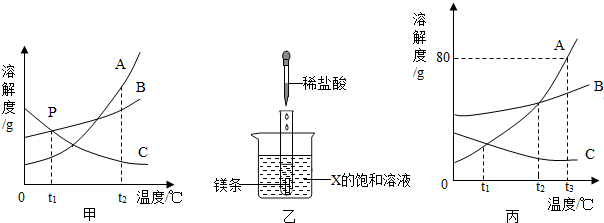
(1)在甲图中,t3℃时,A、B、C三种物质中,溶解度最大的物质是
t℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法
要将B物质从它的饱和溶液中析出,应采用的方法是
(2)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种?
(3)丙图中,S表示物质的溶解度,在
t3℃时,A物质的饱和溶液中溶质的质量分数为

考点:固体溶解度曲线及其作用,溶解时的吸热或放热现象,饱和溶液和不饱和溶液相互转变的方法,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)据溶解度曲线可比较同一温度下不同物质的溶解度,溶解度曲线的交点表示该温度下二者的溶解度相等,溶解度随温度升高而减小的物质升温有溶质析出;
不饱和溶液变为饱和溶液的一般方法是:增加溶质、蒸发溶剂、降温,B的溶解度随温度降低而减小,所以要从其溶液中得到晶体,采取冷却降温的方法;
(2)镁带与盐酸反应放热,使溶液温度升高,烧杯中出现浑浊,说明物质的溶解度随温度升高而减小;
(3)据溶解度曲线比较同一温度时物质的溶解度大小,饱和溶液中溶质的质量分数=
×100%,并结合该温度下A的溶解度分析解答.
不饱和溶液变为饱和溶液的一般方法是:增加溶质、蒸发溶剂、降温,B的溶解度随温度降低而减小,所以要从其溶液中得到晶体,采取冷却降温的方法;
(2)镁带与盐酸反应放热,使溶液温度升高,烧杯中出现浑浊,说明物质的溶解度随温度升高而减小;
(3)据溶解度曲线比较同一温度时物质的溶解度大小,饱和溶液中溶质的质量分数=
| 溶解度 |
| 溶解度+100g |
解答:解:(1)在甲图中,t3℃时,A、B、C三种物质中,溶解度最大的物质是 A,P点所表示的含义为t1℃时A、C两种物质的溶解度相等;随着温度的升高,A、B、C三种物质的饱和溶液中有溶质从溶液中析出的是 C,因为C的溶解度随温度升高而减小;
B的溶解度随温度降低而减小,所以t℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法是:加入B、蒸发溶剂或降温;
要将B物质从它的饱和溶液中析出,应采用的方法是冷却其饱和溶液;
(2)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时放热,烧杯中出现浑浊,说明物质的溶解度随温度升高而减小,则X可能为C,因为C的溶解度随温度升高而减小;
(3)丙图中,S表示物质的溶解度,在t2℃时SA=SB>SC;饱和溶液中溶质的质量分数=
×100%,而t3℃时,A物质的溶解度是80g,即100g水中最多溶解80g的A,形成饱和溶液的质量是180g,所以饱和溶液中溶质的质量分数为
×100%≈44.4%,90gA物质的饱和溶液中,含有A物质40g;
故答案为:(1)A;t1℃时A、C两种物质的溶解度相等;C;加入B;降温;蒸发溶剂;冷却;
(2)C;
(3)t2;44.4%;40.
B的溶解度随温度降低而减小,所以t℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法是:加入B、蒸发溶剂或降温;
要将B物质从它的饱和溶液中析出,应采用的方法是冷却其饱和溶液;
(2)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时放热,烧杯中出现浑浊,说明物质的溶解度随温度升高而减小,则X可能为C,因为C的溶解度随温度升高而减小;
(3)丙图中,S表示物质的溶解度,在t2℃时SA=SB>SC;饱和溶液中溶质的质量分数=
| 溶解度 |
| 溶解度+100g |
| 80g |
| 180g |
故答案为:(1)A;t1℃时A、C两种物质的溶解度相等;C;加入B;降温;蒸发溶剂;冷却;
(2)C;
(3)t2;44.4%;40.
点评:本题较综合的考查了溶解度、溶解度曲线、溶质质量分数的相关知识,掌握相关知识才能结合题意灵活解答.

练习册系列答案
相关题目
下列是我们日常生活中接触到的物质,其中属于纯净物的是( )
| A、洁净的空气 | B、碘酒 |
| C、可口可乐 | D、氧气 |
下列物质的名称、俗名与化学式完全对应的是( )
| A、氯化钠 食盐 NaCl2 |
| B、氢氧化钙 生石灰 CaO |
| C、碳酸氢钠 纯碱 NaHCO3 |
| D、氢氧化钠 烧碱 NaOH |
下列物质中由原子构成的是( )
| A、水 | B、氧气 | C、氦气 | D、二氧化硫 |
保护环境,节约资源,从我做起.下列做法不符合这一理念的是( )
| A、纸张要双面使用 |
| B、随手关闭水龙头 |
| C、尽量不用一次性物品 |
| D、少用自动铅笔,多用木制铅笔 |
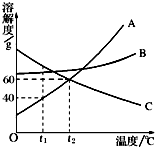 右图是 A、B、C三种物质的溶解度曲线.请回答:
右图是 A、B、C三种物质的溶解度曲线.请回答: