题目内容
【题目】鸡蛋壳主要成分为碳酸钙,小东同学为测定鸡蛋壳中钙元素的质量分数,设计了如下实验。取25 g鸡蛋壳样品于烧杯中,将188.8 g稀盐酸缓慢加入样品中(杂质不溶于水,也不与酸发生反应)。测得烧杯内剩余固体质量与加入稀盐酸质量关系如图:
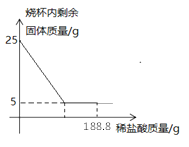
根据图示回答下列问题:
(1)鸡蛋壳样品中碳酸钙的质量为__________g。
(2)鸡蛋壳样品中钙元素的质量分数为__________。
(3)完全加入稀盐酸后,溶液中氯化钙的质量分数为_________?
【答案】 20g 32% 11.1%
【解析】本题考查了根据化学方程式的计算。认真审题,弄清关系图中数据与化学反应的关系是解题的基础。
(1)根据关系图可知,鸡蛋壳样品中碳酸钙的质量=25g-5g=20g;
(2)鸡蛋壳样品中钙元素的质量=20g×![]() ×100%=8g;鸡蛋壳样品中钙元素的质量分数=
×100%=8g;鸡蛋壳样品中钙元素的质量分数=![]() ×100%=32%;
×100%=32%;
(3)设:20g的碳酸钙与盐酸反应能生成氯化钙的质量为x,二氧化碳的质量为y。
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
20g x y
![]()
![]() x=22.2g
x=22.2g
![]() y=8.8g
y=8.8g
完全加入稀盐酸后,溶液中氯化钙的质量分数=![]() ×100%=11.1%。
×100%=11.1%。

【题目】请参与下列探究实验:
(实验探究)
步骤 | 实验操作 | 实验现象 | 结论或解释 |
(1) | 用玻棒分别蘸取95%的酒精、蒸馏水置于火焰上。 | 酒精_______,蒸馏水_______。 | 结论:酒精是可燃物,水不是可燃物。 |
(2) | 在铁片两端放大小相同的硬纸片、乒乓球碎片,在铁片中间加热。 | 乒乓球碎片先燃烧、硬纸片后燃烧。 | 结论:乒乓球碎片的________比硬纸片的低。 |
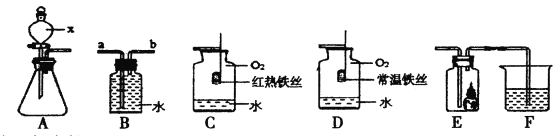
(3) | 在右图中打开分液漏斗的旋塞 | ①溶液中产生气泡;②蜡烛火焰a_____填“先于”“后于”)b熄灭。 | 现象②的原因是:CO2不助燃;___________。 |
(4) | 用大烧杯罩住高低两支点燃的蜡烛。 | ①烧杯底部变黑;②蜡烛火焰d比c先熄灭。 | CO2不助燃,蜡烛不完全燃烧;d先熄灭的原因是:_______。 |
(拓展)堆积的面粉不容易点燃,即使少量点燃也只是小火燃烧;如果把面粉撒向空中遇火星可能会发生爆炸。“小火燃烧”和“发生爆炸”的原因分别是:_______________。
【题目】西大附中初三化学兴趣小组同学开展了下列实验:取刚降到地面的雨水水样通过pH计(测pH的仪器)每隔几分钟测一次pH,测得的结果如下表:
测定时间 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 |
雨水样品的pH | 4.95 | 4.94 | 4.92 | 4.88 | 4.86 | 4.85 |
(1)该雨水__________(填“是”或者“不是”)酸雨。
(2)导致正常雨水呈酸性的气体可能是__________________。
(3)在测定期间雨水的酸性逐渐__________(填“增强”或者“减弱”)。
(4)乙醇作燃料可一定程度缓解酸雨污染,请写出乙醇燃烧的方程式__________。