题目内容
(2012?道外区二模)工业上利用海水提取食盐的过程:
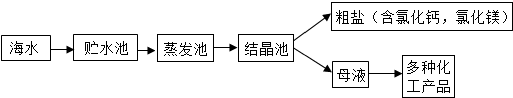
[提出问题]析出的粗盐中含有CaCl2和MgCl2吗?
化学课外小组的同学取粗盐,并进行如下实验:
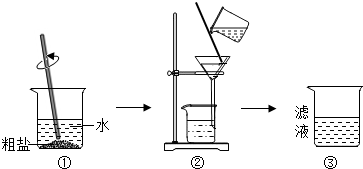
[进行假设]滤液中含有CaCl2和MgCl2,其它杂质不干扰实验现象
[实验与评价]为了证明假设成立,大家一致认为只需证明Ca2+和Mg2+即可
小明设计的方案是:取烧杯③中的溶液,向其中滴加氢氧化钠溶液,若产生白色沉淀,过滤,向所得滤液中再滴加碳酸钠溶液,再次产生白色沉淀,则假设成立,请你进行评价①
小刚的方案是:利用不同于小明的一种无色溶液和一种无色气体设计方案,若他的方案正确,请你猜出他的方案可能是②
[反思交流]在对粗盐混合液过滤时,过滤浑浊,原因可能是③
[拓展应用]工业上得到粗盐后,为了除去氯化钙和氯化镁等杂质,而得到精盐氯化钠,采取有关溶液的知识除杂,方法是④

[提出问题]析出的粗盐中含有CaCl2和MgCl2吗?
化学课外小组的同学取粗盐,并进行如下实验:

[进行假设]滤液中含有CaCl2和MgCl2,其它杂质不干扰实验现象
[实验与评价]为了证明假设成立,大家一致认为只需证明Ca2+和Mg2+即可
小明设计的方案是:取烧杯③中的溶液,向其中滴加氢氧化钠溶液,若产生白色沉淀,过滤,向所得滤液中再滴加碳酸钠溶液,再次产生白色沉淀,则假设成立,请你进行评价①
该实验方案应该加入过量的氢氧化钠溶液
该实验方案应该加入过量的氢氧化钠溶液
;小刚的方案是:利用不同于小明的一种无色溶液和一种无色气体设计方案,若他的方案正确,请你猜出他的方案可能是②
取烧杯③中的溶液,向其中滴加过量氢氧化钠溶液,若产生白色沉淀,过滤,向所得滤液中通入二氧化碳气体,再次产生白色沉淀,则假设成立
取烧杯③中的溶液,向其中滴加过量氢氧化钠溶液,若产生白色沉淀,过滤,向所得滤液中通入二氧化碳气体,再次产生白色沉淀,则假设成立
;[反思交流]在对粗盐混合液过滤时,过滤浑浊,原因可能是③
滤纸破损或过滤时液面高于滤纸的边缘等
滤纸破损或过滤时液面高于滤纸的边缘等
,[拓展应用]工业上得到粗盐后,为了除去氯化钙和氯化镁等杂质,而得到精盐氯化钠,采取有关溶液的知识除杂,方法是④
将粗盐加水溶解,加过量氢氧化钠溶液和过量碳酸钠溶液后充分反应后过滤,然后向滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠
将粗盐加水溶解,加过量氢氧化钠溶液和过量碳酸钠溶液后充分反应后过滤,然后向滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠
.分析:[实验与评价]根据加入的氢氧化钠溶液如果没有足量,那么剩余的镁离子可以与碳酸钠溶液反应生成碳酸镁沉淀影响对钙离子的检验进行解答;
根据氢氧化钠溶液能和氯化镁反应生成氢氧化镁沉淀以及二氧化碳能使钙离子以碳酸钙的形式沉淀进行解答;
[反思交流]根据过滤的注意事项进行解答;
[拓展应用]根据用过量氢氧化钠溶液除去氯化镁、用过量碳酸钠溶液除去氯化钙,然后过滤后在滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠进行解答.
根据氢氧化钠溶液能和氯化镁反应生成氢氧化镁沉淀以及二氧化碳能使钙离子以碳酸钙的形式沉淀进行解答;
[反思交流]根据过滤的注意事项进行解答;
[拓展应用]根据用过量氢氧化钠溶液除去氯化镁、用过量碳酸钠溶液除去氯化钙,然后过滤后在滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠进行解答.
解答:解:[实验与评价]加入的氢氧化钠溶液如果没有足量,那么剩余的镁离子可以与碳酸钠溶液反应生成碳酸镁沉淀影响对钙离子的检验,所以该实验方案应该加入过量的氢氧化钠溶液;故填:该实验方案应该加入过量的氢氧化钠溶液;
氢氧化钠溶液能和氯化镁反应生成氢氧化镁沉淀,二氧化碳能使钙离子以碳酸钙的形式沉淀,所以小刚的方案是:取烧杯③中的溶液,向其中滴加过量氢氧化钠溶液,若产生白色沉淀,过滤,向所得滤液中通入二氧化碳气体,再次产生白色沉淀,则假设成立;故填:取烧杯③中的溶液,向其中滴加过量氢氧化钠溶液,若产生白色沉淀,过滤,向所得滤液中通入二氧化碳气体,再次产生白色沉淀,则假设成立;
[反思交流]在对粗盐混合液过滤时,过滤浑浊,原因可能是:滤纸破损或过滤时液面高于滤纸的边缘等;故填:滤纸破损或过滤时液面高于滤纸的边缘等;
[拓展应用]用过量氢氧化钠溶液除去氯化镁、用过量碳酸钠溶液除去氯化钙,然后过滤后在滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠进,所以方法是将粗盐加水溶解,加过量氢氧化钠溶液和过量碳酸钠溶液后充分反应后过滤,然后向滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠.故填:将粗盐加水溶解,加过量氢氧化钠溶液和过量碳酸钠溶液后充分反应后过滤,然后向滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠.
氢氧化钠溶液能和氯化镁反应生成氢氧化镁沉淀,二氧化碳能使钙离子以碳酸钙的形式沉淀,所以小刚的方案是:取烧杯③中的溶液,向其中滴加过量氢氧化钠溶液,若产生白色沉淀,过滤,向所得滤液中通入二氧化碳气体,再次产生白色沉淀,则假设成立;故填:取烧杯③中的溶液,向其中滴加过量氢氧化钠溶液,若产生白色沉淀,过滤,向所得滤液中通入二氧化碳气体,再次产生白色沉淀,则假设成立;
[反思交流]在对粗盐混合液过滤时,过滤浑浊,原因可能是:滤纸破损或过滤时液面高于滤纸的边缘等;故填:滤纸破损或过滤时液面高于滤纸的边缘等;
[拓展应用]用过量氢氧化钠溶液除去氯化镁、用过量碳酸钠溶液除去氯化钙,然后过滤后在滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠进,所以方法是将粗盐加水溶解,加过量氢氧化钠溶液和过量碳酸钠溶液后充分反应后过滤,然后向滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠.故填:将粗盐加水溶解,加过量氢氧化钠溶液和过量碳酸钠溶液后充分反应后过滤,然后向滤液中加入盐酸除去多余的氢氧化钠和碳酸钠,蒸发结晶即可得到纯净的氯化钠.
点评:化学来源于生产、生活,又服务于生产、生活,本题主要考查氯化钠与粗盐提纯的步骤、工业制镁的步骤以及实验方案评价.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
 (2012?道外区二模)哈尔滨中华巴洛克建筑群位于道外区靖宇街一侧,是全世界保存最完整、最大的建筑群落.在修复时使用了大量的化学材料.据此请你推测下列说法错误的是( )
(2012?道外区二模)哈尔滨中华巴洛克建筑群位于道外区靖宇街一侧,是全世界保存最完整、最大的建筑群落.在修复时使用了大量的化学材料.据此请你推测下列说法错误的是( )