题目内容
菱铁矿的主要成分是FeCO3,下列关于FeCO3的说法中正确的是( )
| A、由原子直接构成 | ||
| B、碳、氧元素的质量比是1:3 | ||
| C、铁元素的化合价为+3价 | ||
D、Fe元素的质量分数是
|
考点:化学式的书写及意义,分子、原子、离子、元素与物质之间的关系,有关元素化合价的计算,元素质量比的计算,元素的质量分数计算
专题:化学用语和质量守恒定律
分析:A.根据物质的结构来分析;B.根据化合物中元素质量比的计算方法来分析;C.根据化合物中元素化合价的计算方法来分析;D.根据化合物中元素质量分数的计算方法来分析.
解答:解:A.FeCO3是由亚铁离子和碳酸根离子构成的,不是由原子直接构成的,故错误;
B.FeCO3中碳、氧元素的质量比为:12:(16×3)=3:12;故错误;
C.FeCO3中,碳酸根显-2价,根据化合物中各元素正负化合价的代数和为零原则可知,铁元素显+2价,故错误;
D.FeCO3中Fe元素的质量分数为:
×100%=48.3%,故正确.
故选D.
B.FeCO3中碳、氧元素的质量比为:12:(16×3)=3:12;故错误;
C.FeCO3中,碳酸根显-2价,根据化合物中各元素正负化合价的代数和为零原则可知,铁元素显+2价,故错误;
D.FeCO3中Fe元素的质量分数为:
| 56 |
| 56+12+16×3 |
故选D.
点评:本题主要考查学生根据化学式确定物质元素及根据组成物质元素之间的质量关系进行分析解题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
对于化学反应A+B→C+D的下列说法中正确的是( )
| A、若生成物C和D分别为盐和水,则该反应一定是中和反应 |
| B、若A和C是单质,B和D是化合物,则该反应一定是置换反应 |
| C、若A是可溶性碱,B是可溶性盐,则C和D不可能是两种沉淀 |
| D、若A、B、C、D都是化合物,则该反应一定是复分解反应 |
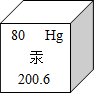 2014年1月18日,我国最大节能灯管产地浙江临安遭汞污染,如图为汞元素周期表中的一格,下列有关说法不正确的是( )
2014年1月18日,我国最大节能灯管产地浙江临安遭汞污染,如图为汞元素周期表中的一格,下列有关说法不正确的是( )| A、该元素的原子序数为80 |
| B、该元素的相对原子质量为200.6 |
| C、该元素的原子核外有80个电子 |
| D、体温计中的汞柱随温度的升高而上升,是因为温度越高汞原子体积越大 |
下列微粒符号中,对“2”的含义理解正确的是( )
| A、2Mg表示2个镁元素 |
| B、2CO 表示2个一氧化碳分子 |
| C、Zn2+ 表示Zn的化合价为+2价 |
| D、S2-表示核外电子数为2个 |
2013年12月,山东发生了“夺命快递”事件,涉及到有毒化学品氟乙酸甲酯(FCH2COOCH3).下列关于氟乙酸甲酯的说法正确的是( )
| A、氟乙酸甲酯中碳元素、氢元素的质量比为3:5 |
| B、氟乙酸甲酯由碳、氢、氧三种元素组成 |
| C、氟乙酸甲酯分子中有5个碳原子、13个氢原子、1个氮原子和2个氧原子 |
| D、氟乙酸甲酯属于有机物 |
下列物质中属于纯净物的是( )
| A、矿泉水 | B、天然气 |
| C、过氧化氢溶液 | D、冰水混合体 |
某学生用托盘天平称量5.5gKCl晶体(1g以下用游码),称量时误将药品与砝码的位置颠倒.该学生所称KCl的实际质量是( )
| A、6 g |
| B、5.5 g |
| C、5.0 g |
| D、4.5 g |
 化学是一门研究物质的组成、结构、以及变化规律的科学,它与人类进步和社会发展有着密切的联系.
化学是一门研究物质的组成、结构、以及变化规律的科学,它与人类进步和社会发展有着密切的联系.