题目内容
科学家经过多年研究证明,有一些同学爱吃的小包装零食中,含一定量的有毒、有害、致病的化学物质,如某些油炸食品中含有致癌物质丙烯酰胺(C3H5ON).请你根据丙烯酰胺(C3H5ON)的化学式计算后填写:(1)丙烯酰胺(C3H5ON)的相对分子质量为______;
(2)碳、氢、氮元素的质量比是______;
(3)氢元素的质量分数为______.
(4)已知亚硝酸钠(NaNO2)也是一种有毒的致癌物质,请计算13.8g亚硝酸钠与多少丙烯酰胺中含的氮元素质量相等?
【答案】分析:(1)根据丙烯酰胺(C3H5ON)的化学式可知,其相对分子质量=(碳的相对原子质量×碳原子个数)+(氢的相对原子质量×氢原子个数)+(氧的相对原子质量×氧原子个数)+(氮的相对原子质量×氮原子个数);
(2)碳、氢、氮元素的质量比=(碳的相对原子质量×碳原子个数):(氢的相对原子质量×氢原子个数):(氮的相对原子质量×氮原子个数)
(3)氢元素的质量分数为: ×100%;
×100%;
(4)根据氮元素质量相等列出方程式,就可计算出丙烯酰胺的质量.
解答:解:(1)根据丙烯酰胺(C3H5ON)的化学式可知,其相对分子质量=12×3+1×5+16+14=71;故答案为:71;
(2)碳、氢、氮元素的质量比=(12×3):(1×5):14=36:5:14;故答案为:36:5:14;
(3)丙烯酰胺中氢元素的质量分数为: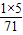 ×100%≈7.0%;故答案为:7.0%;
×100%≈7.0%;故答案为:7.0%;
(4)解:设与13.8g亚硝酸钠含的氮元素质量相等的丙烯酰胺的质量为x,
13.8g×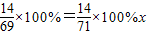
解之得:x=14.2%.
答:13.8g亚硝酸钠与14.2g丙烯酰胺中含的氮元素质量相等.
点评:本题主要考查学生运用化学式和盐酸的质量分数公式等综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
(2)碳、氢、氮元素的质量比=(碳的相对原子质量×碳原子个数):(氢的相对原子质量×氢原子个数):(氮的相对原子质量×氮原子个数)
(3)氢元素的质量分数为:
 ×100%;
×100%;(4)根据氮元素质量相等列出方程式,就可计算出丙烯酰胺的质量.
解答:解:(1)根据丙烯酰胺(C3H5ON)的化学式可知,其相对分子质量=12×3+1×5+16+14=71;故答案为:71;
(2)碳、氢、氮元素的质量比=(12×3):(1×5):14=36:5:14;故答案为:36:5:14;
(3)丙烯酰胺中氢元素的质量分数为:
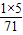 ×100%≈7.0%;故答案为:7.0%;
×100%≈7.0%;故答案为:7.0%;(4)解:设与13.8g亚硝酸钠含的氮元素质量相等的丙烯酰胺的质量为x,
13.8g×
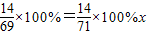
解之得:x=14.2%.
答:13.8g亚硝酸钠与14.2g丙烯酰胺中含的氮元素质量相等.
点评:本题主要考查学生运用化学式和盐酸的质量分数公式等综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目