题目内容
化学小组同学取某黄铜(铜和锌的合金)样品进行如下实验,他们取该黄铜样品碎屑50g,把200g稀硫酸分4次加入到该样品中,测得数据记录如下表:| | 第1次 | 第2次 | 第3次 | 第4次 |
| 加人稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 43.5 | 37.0 | 33.75 | 33.75 |
(2) 计算生成氢气的总质量(写出计算过程)。
(1)125
(2)0.5g解析:
⑴ 125 -------------------------------(1分)
(2) 解:设生成氢气的总质量为x
Zn + H2SO4 ="=" ZnSO4 + H2↑
2
(50-33.75)g x -------------------(1分)
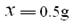 ---------------------------------(1分)
---------------------------------(1分)答:生成氢气的总质量为0.5g。

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
化学小组同学取某黄铜(铜和锌的合金)样品进行如下实验,他们取该黄铜样品碎屑50g,把200g稀硫酸分4次加入到该样品中,测得数据记录如下表:
(1)当加入稀硫酸的质量为 g时,反应恰好完成.
(2)计算生成氢气的总质量(写出计算过程).
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 43.5 | 37.0 | 33.75 | 33.75 |
(2)计算生成氢气的总质量(写出计算过程).
(3分)化学小组同学取某黄铜(铜和锌的合金)样品进行如下实验,他们取该黄铜样品碎屑50g,把200g稀硫酸分4次加入到该样品中,测得数据记录如下表:
|
| 第1次 | 第2次 | 第3次 | 第4次 |
| 加人稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 43.5 | 37.0 | 33.75 | 33.75 |
(1) 当加入稀硫酸的质量为 g时,反应恰好完成。
(2) 计算生成氢气的总质量(写出计算过程)。
化学小组同学取某黄铜(铜和锌的合金)样品进行如下实验,他们取该黄铜样品碎屑50g,把200g稀硫酸分4次加入到该样品中,测得数据记录如下表:
| 第1次 | 第2次 | 第3次 | 第4 | |
| 加人稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 43.5 | 37.0 | 33.75 | 33.75 |
(1) 当加入稀硫酸的质量为 g时,反应恰好完成。
(2) 计算生成氢气的总质量(写出计算过程)。
